
人们常用_____________来表示空气质量。空气污染指数是根据空气中_______、_________和________等污染物的浓度计算出来的数值。
科目:高中化学 来源:2014-2015学年福建省福州市高三上学期期末考试化学试卷(解析版) 题型:选择题
以下方法可用于工业冶炼金属的是
A.电解熔融AlCl3获取金属铝 B.电解MgCl2溶液获取金属镁
C.用CO还原铁矿石来获取金属铁 D. 电解饱和食盐水来获取金属钠
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高二上学期期末化学试卷(解析版) 题型:选择题
用石墨电极电解500mLNaNO3和Cu(NO3)2的混合溶液。通电一段时间后,阴、阳两极逸出的气体在标准状况下的体积分别为11.2L和8.4L,求原溶液中Cu2+的物质的量浓度(假设溶液的体积不变):
A.1.25 mol?L-1 B.2.5 mol?L-1
C.0.50 mol?L-1 D.1.0 mol?L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高二上学期期末化学试卷(解析版) 题型:选择题
下列说法正确的是
A.有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大
B.催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率
C.增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
D.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高二上学期期末化学试卷(解析版) 题型:选择题
下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C(s)+ O2(g)=CO(g) ΔH=-110.5kJ·mol-1 (燃烧热)
O2(g)=CO(g) ΔH=-110.5kJ·mol-1 (燃烧热)
B.2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1(反应热)
C.C2H5OH+3O2=2CO2+3H2O ΔH=-1368.8 kJ·mol-1(反应热)
D.2NaOH(aq)+H2SO4(aq)=Na2SO4 (aq)+2H2O(l) ΔH=-114.6 kJ·mol-1(中和热)
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
我国政府为了消除碘缺乏病,在食用盐中均加入一定量的“碘”。下列关于“碘盐”叙述正确的是
A.“碘盐”应保存在阴凉处 B.“碘盐”就是“I2+NaCl”
C.“碘盐”就是NaI D.使用“碘盐”时宜高温煎炒
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
打雷放电时,空气中有少量氧气会转化成臭氧(3O2=2O3),使空气变得更加清新。下列有关说法中正确的是
A.该变化是物理变化 B.O2与O3都是单质
C.O2与O3是相同的物质 D.O2与O3的性质完全一样
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
硬水和软水的本质区别是
A.硬水浑浊、软水澄清
B.硬水含有杂质、软水含杂质少
C.硬水是不纯净水,软水是纯净水
D.硬水含有较多可溶性钙镁化合物、软水不含或含少量可溶性钙镁化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:填空题
(10分)氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。常用电离常数Kb和电离度α来定量表示氨水的电离程度,它们均可通过各浓度氨水对应的c(OH-)进行换算。下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50 mL碱式滴定管、100mL烧杯、 0.10 mol·L-1 氨水
【实验数据】(不必填表格)
烧杯号 | V氨水 (mL) | V水(mL) | c (NH3·H2O) (mol·L-1) | c(OH-) | Kb | α |
1 | 50.00 | 0.00 | 1.34×10-3 | |||
2 | 25.00 | 25.00 | 9.48×10-4 | |||
3 | 5.00 | 45.00 | 4.24×10-4 |
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb 。
。
(2)用0.10mol·L—1盐酸分别滴定20.00mL0.10mol·L—1
的NaOH溶液和20.00mL0.10mol·L—1氨水所得的滴定曲线如图。
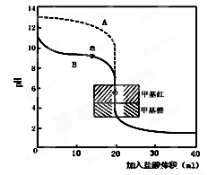
请指出盐酸滴定氨水的曲线为 (填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 。
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料。其总反应式为4NH3+3O2= 2N2+6H2O,正极上的电极反应式为O2+2H2O+4e—=4OH—,则负极上的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com