
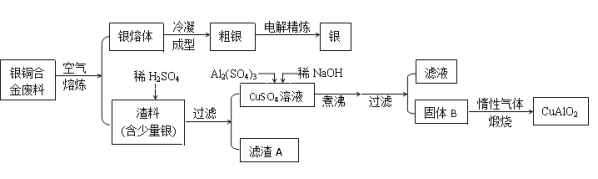
【题目】从银铜合金废料中回收银并制备铜化工产品的工艺如下:
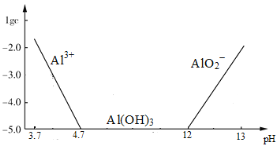
已知:①铝元素在溶液中的存在形态与溶液pH的关系如图所示。
②室温时,Cu(OH)2的溶度积Ksp=2.0×10-20,当溶液中某种离子浓度小于1.0×10-5mol/L时,认为该离子沉淀完全,![]() 。
。
③Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
请回答下列问题:
(1)电解精炼银时,粗银做 极(填“阴”或“阳”),电解质选用________溶液,阴极电极反应为 。
(2)在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在 ,若控制不当,使NaOH过量可能会引起的反应的离子方程式为 。
(3) 煅烧过程中发生多步反应,写出最终生成CuAlO2的反应的化学方程式: 。
(4)若银铜合金中铜的质量分数为64%,理论上1.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液 L。
【答案】
(1)阳;AgNO3;Ag++e-=Ag;
(2)6.65-12;Al(OH)3+OH-=AlO2-+2H2O;
(3)2Al2O3+4CuO=4CuAlO2+O2;(4)5;
【解析】
试题分析:(1)电镀法精炼银时,粗银为阳极,精银为阴极,硝酸银作电解质溶液,阳极上失电子变成离子进入溶液了:Ag-e-=Ag+,阴极银离子得到电子形成单质银:Ag++e-=Ag,故答案为:阳;AgNO3;Ag++e-=Ag;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO,在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在铝离子和铜离子全部沉淀,氢氧化铝沉淀完全PH=12,室温时,Cu(OH)2的溶度积Ksp=2.0×10-20.(lg5=0.7),据此计算全部沉淀的PH,c2(OH-)=![]() =2×10-15,c(H+)=10-6.65,PH=6.65,在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在为:6.65-12,氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:6.65-12; Al(OH)3+OH-=AlO2-+2H2O;
=2×10-15,c(H+)=10-6.65,PH=6.65,在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在为:6.65-12,氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:6.65-12; Al(OH)3+OH-=AlO2-+2H2O;
(3)反应前Cu为+2价,反应后为+1,化合价降低1,Al化合价没有变化,所以氧元素的化合价升高,生成氧气,反应前氧为-2价,反应后为0,化合价升高2,两者的最小公倍数是2,再根据原子守恒得:4CuO+2Al2O3=4CuAlO2+O2↑,故答案为:4CuO+2Al2O3=4CuAlO2+O2↑;
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=![]() =10.0mol,则CuAlO2为10.0mol,由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×
=10.0mol,则CuAlO2为10.0mol,由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×![]() =5.0mol,所以需要体积为
=5.0mol,所以需要体积为![]() =5L,故答案为:5。
=5L,故答案为:5。


科目:高中化学 来源: 题型:
【题目】纯铁的熔点为1535℃,而在高炉中炼铁时生铁(含碳量较高的铁的合金)在1200℃左右就熔化了,这是因为
A. 铁的纯度越高熔点越低
B. 合金的熔点比其成分物质的熔点高
C. 因为形成了铁碳合金,所以熔点变低
D. 在高炉中熔化的过程中发生了化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿泉水标签上印有主要的矿物质成分如下(单位为mg/L):Ca 20,K 39,Mg 3,Zn 0.06,F 0.02等,这里的 Ca,K,Mg,Zn,F是指 ( )
A. 单质 B. 元素 C. 金属离子 D. 分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国农业因遭受酸雨而造成的损失每年高达15亿元以上。为了有效控制酸雨,目前国务院已颁布了多项法规。以下各种物质哪种与酸雨的形成无关 ( )
A. SO2 B. NO C. NO2 D. CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,前者加入后者时,无论前者是否过量,都能用同一离子方程式表示的是(还原性Fe2+> Br-> C1-) ( )
A. 稀盐酸,碳酸钠溶液 B. 稀盐酸,碳酸氢钠溶液
C. 碳酸氢钠溶液,澄清石灰水 D. 氯水,溴化亚铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选修3——物质结构与性质
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素,相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是 ,离子化合物YX5的电子式是 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐),A晶体的晶胞为正方体(如图1)。
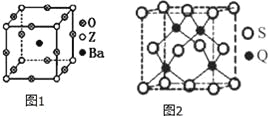
①制备A的化学反应方程式是 ;
②在A晶体中,Z的配位数为 ;
(4)R2+离子的外围电子层电子排布式为 。R2O的熔点比R2S的 (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B,B晶体的晶胞为正方体(如图2),若晶胞棱长为5.4×10-8cm,则晶胞密度为 gcm﹣3(列式并计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不符合生产实际的是( )
A. 在镀件上电镀锌,用锌作阳极
B. 电解法精炼粗铜,用纯铜作阴极
C. 电解饱和食盐水制烧,用涂镍碳钢网作阴极
D. 电解熔融的氧化铝制取金属铝,用铁作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用乙烯和氯气在适当的条件下反应制取四氯乙烷,这一过程中所要经历的反应及耗用氯气的量是(设乙烯为1mol ,反应产物中的有机物只是四氯乙烷) ( )
A. 取代,4 mol Cl2 B.加成,2 mol Cl2
C.加成、取代,2 mol Cl2 D.加成、取代,3 mol Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的使用合理的是
A.碳酸钠用于治疗胃酸过多
B.婴儿食品应添加着色剂,以增加婴儿对食物的兴趣
C.维生素C可防治坏血病,因而我们需要大量补充维生素C
D.药物可以帮助我们战胜疾病,但我们仍需合理用药
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com