
(10分)A、B、C、D分别为(NH4)2SO4、Ba(OH)2、AlCl3、Na2CO3 4种物质中的1种,现进行如下实验:
①实验测得A溶液和D溶液显碱性,B溶液和C溶液显酸性;
②A溶液和D溶液混合可生成沉淀甲
③足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体;
请回答:
(1)B的化学式为________;沉淀甲的化学式为________。
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为 。
(3)加热蒸干C溶液并灼烧,最后所得固体为________(填化学式)。
(4)D溶液中各离子浓度由大到小的顺序为 。
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2·L-2,沉淀乙的Ksp=1.1×10-10 mol2·L-2。将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙。写出该转化反应的离子方程式: 。
(1) (NH4)2SO4 (1分)BaCO3(1分)
(2)Ba2+ +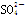 +2 OH-+
+2 OH-+
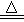 BaSO4↓+2NH3↑+2 H2O(2分)
BaSO4↓+2NH3↑+2 H2O(2分)
(3)Al2O3 (2分)
(4)c(Na+) > c(CO32-)> c(OH-) >c(HCO3-)>c(H+) (2分)
(5)BaCO3 (s)+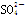 (aq)===BaSO4 (s)+CO32-(aq) (2分)
(aq)===BaSO4 (s)+CO32-(aq) (2分)
【解析】
试题分析:(NH4)2SO4为强酸弱碱盐,溶液显酸性;Ba(OH)2为强碱,溶液显碱性;AlCl3为强酸弱碱盐,溶液显酸性;Na2CO3为强碱弱酸盐,溶液显碱性;A溶液和D溶液显碱性,B溶液和C溶液显酸性;A溶液和D溶液混合可生成沉淀甲,所以甲为BaCO3;A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体;刺激性气味气体为氨气,所以A为Ba(OH)2,B为(NH4)2SO4;C为AlCl3;D为Na2CO3;A、B反应的离子方程式为Ba2+ +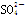 +2 OH-+
+2 OH-+
 BaSO4↓+2NH3↑+2 H2O;沉淀乙为硫酸钡AlCl3溶液加热促进Al3+水解平衡右移,所以加热蒸干得到氢氧化铝沉淀,灼烧得到氧化铝;Na2CO3溶液中CO32-水解, CO32-+H2O
BaSO4↓+2NH3↑+2 H2O;沉淀乙为硫酸钡AlCl3溶液加热促进Al3+水解平衡右移,所以加热蒸干得到氢氧化铝沉淀,灼烧得到氧化铝;Na2CO3溶液中CO32-水解, CO32-+H2O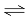 HCO3-+OH-,水能电离出OH-,所以c(Na+) > c(CO32-)> c(OH-) >c(HCO3-)>c(H+);沉淀甲转化为沉淀乙的离子方程式为BaCO3 (s)+
HCO3-+OH-,水能电离出OH-,所以c(Na+) > c(CO32-)> c(OH-) >c(HCO3-)>c(H+);沉淀甲转化为沉淀乙的离子方程式为BaCO3 (s)+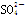 (aq)===BaSO4 (s)+CO32-(aq)
(aq)===BaSO4 (s)+CO32-(aq)
考点:本题考查盐的水解、离子反应、沉淀溶解平衡。


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:填空题
(8分)(1)9.2g氮的氧化物NOx中含有N原子数为0.2 mol,则NOx的摩尔质量为___________,x数值为_______,这些质量的NOx在标准状况的体积约为_______。
(2)V L Fe2(SO4)3溶液中含有a g SO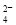 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
在相同条件下,燃烧时对大气污染程度最小的燃料是
A.液化气 B.煤油 C.煤球 D.木柴
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关,下列有关说法不正确的是( )
A.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印机属于“低碳生活”方式
B.我国神七宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C.食品保鲜膜、一次性食品袋的主要成分是聚氯乙烯
D.日本福岛核电站爆炸时释放的2种放射性同位素131I与137Cs的中子数不等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.需要加热方能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高二上学期联考化学试卷(解析版) 题型:选择题
某温度下,在一定体积的密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度
如下表,下列说法错误的是
物质 | X | Y | Z | W |
初始浓度/mol·L-1 | 0.5 | 0.6 | 0 | 0 |
平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A.增大压强反应的平衡常数不变,但X的转化率增大
B.该反应的化学方程式为:4X (g)+5Y (g)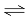 4Z (g)+ 6W (g)
4Z (g)+ 6W (g)
C.反应达到平衡时,X的转化率为80%
D.其它条件不变,若增大Y的起始浓度,X的转化率增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高二上学期联考化学试卷(解析版) 题型:选择题
在体积为1L的密闭容器中发生反应2SO2(g)+O2(g)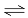 2SO3(g)。达到平衡后,若采用下列措施一段时间后,能增大逆反应速率的是
2SO3(g)。达到平衡后,若采用下列措施一段时间后,能增大逆反应速率的是
A.体积不变,通入NO
B.增大容器容积
C.体积不变,通入大量O2
D.降低体系温度
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高一上学期联考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列说法正确的是
A.0.5mol·L-1 Na2SO4溶液中所含的Na+数为NA
B.常温常压下,4g氦气所含有的质子数为4NA
C.1molCl2与足量Fe反应,转移的电子数为3NA
D.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省乐陵市高二上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下,在0.1mol/LNaOH溶液和0.1mol/L盐酸中水的离子积相等
B.常温下,在水中加入NaOH,水的电离受到抑制,水的离子积减小
C.HCl溶液中无OH-,NaOH溶液中无H+,NaCl溶液中既无OH-也无H+
D.在水溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com