
| 酸 | 碱 | 盐 | 氧化物 | |
| A | H2SO4 | Na2CO3 | NaCl | CO2 |
| B | HCl | NaOH | NaHCO3 | CaO |
| C | CO2 | NH3•H2O | Na2CO3 | CuO |
| D | CH3COOH | KOH | KCl | KClO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物属于盐,氧化物是含有两种元素且其中一种元素是氧元素的化合物,据此分析.
解答 解:A、硫酸电离时生成的阳离子都是氢离子,都属于酸,Na2CO3 是钠离子和碳酸根离子构成的盐,不是碱,NaCl属于盐,CO2属于氧化物,故A错误;
B、HCl水溶液中电离出的阳离子全部是氢离子的化合物为酸,NaOH水溶液中电离出的阴离子全部是氢氧根离子的化合物属于碱,NaHCO3是钠离子和碳酸氢根离子构成属于盐,CaO是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故B正确;
C、CO2是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,NH3•H2O水溶液中电离出的阴离子全部是氢氧根离子的化合物属于碱,Na2CO3 是钠离子和碳酸根离子构成的盐,CuO属于氧化物,故C错误;
D、CH3COOH水溶液中电离出的阳离子全部是氢离子的化合物为酸,KOH水溶液中电离出的阴离子全部是氢氧根离子的化合物属于碱,KCl是钾离子和氯离子构成的盐,KClO3是钾离子和氯酸根离子构成的盐,不是氧化物,故D错误.
故选B,
点评 本题主要考查盐的概念,解答时要分析各种物质的组成,然后再根据酸、碱、盐、氧化物概念的含义进行分析、判断,从而得出正确的结论,题目较简单.


科目:高中化学 来源: 题型:解答题
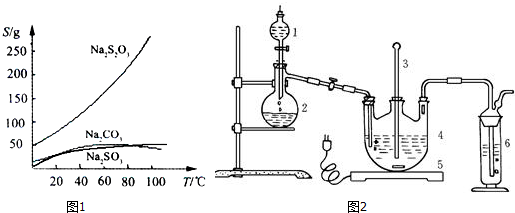

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
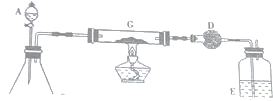
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
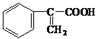 )和甲醇反应制得.
)和甲醇反应制得.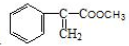
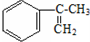 经过四步不同类型的反应制得阿托酸.
经过四步不同类型的反应制得阿托酸.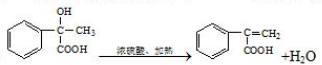 .
.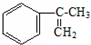 多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式
多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式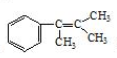 .
.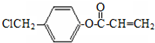 是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为
是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为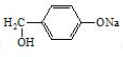 、
、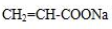 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
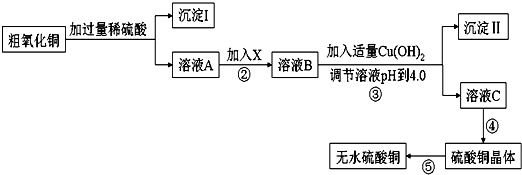
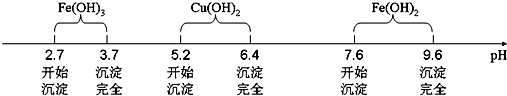
| 滴定次数 | 第一次 | 第二次 | 第三次 |
| 滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
| 滴定滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液操作时,先将分液漏斗中的下层液体放出,再将上层液体接着放出 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| C. | 蒸馏实验中温度计的水银球应插入液态混合物中 | |
| D. | 过滤时玻璃棒的末端应轻轻靠在三层滤纸上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
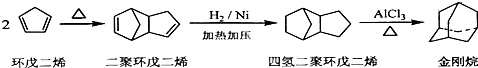

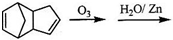
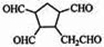
查看答案和解析>>
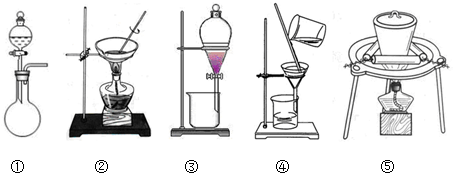
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①③ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com