
将某有机物样品3.0g通入足量的氧气后充分燃烧,在120℃条件下将燃烧后的气体通入足量的浓H2SO4中,浓H2SO4增重1.8g,然后将气体再通入足量的氢氧化钡溶液中,可得到沉淀19.7g(不考虑溶解的沉淀物),此时还有标准状况下的气体2.24L,该气体能用于抢救危重病人.实验测得该有机物蒸气的密度是相同条件下氦气的15倍.求该有机物的分子式和通入氧气的总体积(标准状况)?
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
| 名称 | 性质 |
| 乙二醇 | 无色粘稠吸湿液体,易燃,沸点:196~198℃,与水混溶. |
| 丙酮 | 无色易燃液体,沸点:56.5℃,溶于水及大多数有机溶剂. |
| N,N二甲基甲酰胺(DMF) | 易燃,低毒,沸点:153℃,能与水和大多数有机溶剂混溶. |
| 对苯二甲酸(TPA) | 白色针状结晶或粉末,可燃,熔点:425℃(分解),约在300℃升华,不溶于水,微溶于热乙醇,溶于碱溶液.电离常数:Ka1=3.1×10-4,Ka2=1.5×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
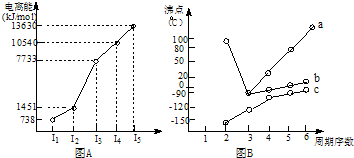
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 | 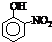 |
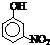 |
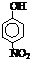 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 判断依据 | 结论(写结构简式)) |
| 核磁共振氢谱有1个峰 | CH3OCH3 CH3OCH3 |
| 核磁共振氢谱有3个峰 | CH3CH2OH CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
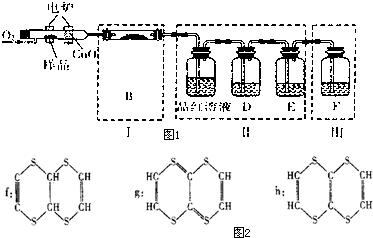 有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分.某化学兴趣小组为验证其组成元素,并探究其分子结构进行了下列实验:
有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分.某化学兴趣小组为验证其组成元素,并探究其分子结构进行了下列实验:查看答案和解析>>
科目:高中化学 来源:2014届辽宁省五校协作体高三(高二期末)摸底考试化学试卷(解析版) 题型:实验题
白菜中含有钙铁等元素,某化学小组设计如下方案测定干白菜中钙元素的质量分数。首先取10.00g干白菜叶,灼烧得白菜灰粉进行下列实验:

(1)实验前要先将干白菜叶样品高温灼烧成灰粉,其主要目的是使样品中的有机物完全分解,使干白菜叶中的钙、铁元素溶解完全,灼烧用到的部分仪器有
A.坩埚 B.蒸发皿 C.玻璃棒 D.泥三角
(2)写出从滤液A→沉淀D的离子反应方程式 。
(3)用KMnO4标准溶液滴定滤液C:先将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.100 0 mol·L-1’的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL。
发生的反应为:
①滴定的过程中,同学们发现一个现象:向C溶液中加入第一滴KMnO4溶液时,需要振摇锥形瓶较长时间才能褪色,当溶液褪色后,再滴入KMnO4溶液,则迅速褪色,直至达到终点;为了加快滴入第一滴KMnO4溶液时的褪色速度,可采取的方法是 .(选择合适的选项)
A.适当加热锥形瓶内溶液 B.在锥形瓶内加少量水
C.在锥形瓶内加适量乙醇 D.在锥形瓶内加入几滴MnSO4溶液
②判断滴定达到终点的方法是 。
(4)原干白菜叶中钙元素的质量分数为 。
(5)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是 。如果沉淀E未洗涤,或未将洗涤液转移回母液,则测得的钙元素质量分数 (填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com