
【题目】根据所学知识,完成下列问题。
(1)用系统命名法给下列有机物命名:
①![]() ___________;②
___________;② ___________。
___________。
(2)分子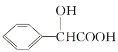 中含有的官能团名称为___________。
中含有的官能团名称为___________。
(3)某有机物分子式为C8H8,且属于芳香烃,已知它可使酸性高锰酸钾溶液和溴水褪色,则该有机物的结构简式为__________。
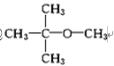
(4)某烃的含氧衍生物可以作为无铅汽油的抗爆震剂,它的相对分子质量为88.0,含碳的质量分数为68.2%,含氢的质量分数为13.6%,红外光谱和核磁共振氢谱显示该分子中有4个甲基,请写出其结构简式______________。
【答案】2-甲基丁烷 3-甲基戊烷 羟基、羧基 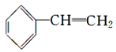
【解析】
(1) 根据主链最长原则选取主链,根据离支链最近给主链碳原子编号;
(2)分子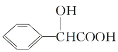 中含有官能团是
中含有官能团是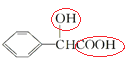 ;
;
(3)分子式为C8H8,不饱和度是5,属于芳香烃说明含有苯环,可使酸性高锰酸钾溶液和溴水褪色,说明侧链含有碳碳双键;
(4)相对分子质量为88.0,含碳的质量分数为68.2%,则碳原子数是![]() ,含氢的质量分数为13.6%,则碳原子数是
,含氢的质量分数为13.6%,则碳原子数是![]() ,氧原子数是
,氧原子数是![]() 。
。
(1)①根据主链最长原则,![]() 主链有4个碳原子,主链第2个碳原子有1个甲基,名称是2-甲基丁烷;②根据主链最长原则,
主链有4个碳原子,主链第2个碳原子有1个甲基,名称是2-甲基丁烷;②根据主链最长原则,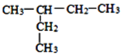 主链有5个碳原子,主链第3个碳原子有1个甲基,名称是3-甲基戊烷;
主链有5个碳原子,主链第3个碳原子有1个甲基,名称是3-甲基戊烷;
(2)分子 中含有官能团是
中含有官能团是 ,官能团名称是羟基、羧基;
,官能团名称是羟基、羧基;
(3)分子式为C8H8,不饱和度是5,属于芳香烃说明含有苯环,可使酸性高锰酸钾溶液和溴水褪色,说明侧链含有碳碳双键,可能结构简式是![]() ;
;
(4)相对分子质量为88.0,含碳的质量分数为68.2%,则碳原子数是![]() ,含氢的质量分数为13.6%,则碳原子数是
,含氢的质量分数为13.6%,则碳原子数是![]() ,氧原子数是
,氧原子数是![]() ,分子式是C5H12O,红外光谱和核磁共振氢谱显示该分子中有4个甲基,其结构简式是
,分子式是C5H12O,红外光谱和核磁共振氢谱显示该分子中有4个甲基,其结构简式是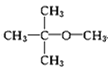 。
。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】如图(Ea表示活化能)是CH4与Cl2生成CH3Cl的部分反应过程中各物质物质的能量变化关系图,下列说法正确的是( )
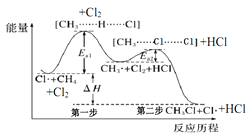
A.Cl·可由Cl2在高温条件下生成,是CH4与Cl2反应的催化剂
B.升高温度,Ea1、Ea2均减小,反应速率加快
C.增大Cl2的浓度,可提高反应速率,但不影响△H的大小
D.第一步反应的速率大于第二步反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐(3PbO·PbSO4·H2O,相对分子质量为990)可用作聚氯乙烯的热稳定剂,不溶于水。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示:
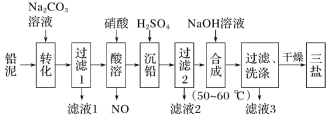
已知:Ksp(PbSO4)=1.82×10-8;Ksp(PbCO3)=1.46×10-13。回答下列问题:
(1)加Na2CO3溶液转化的目的是__。
(2)酸溶时,不直接使用H2SO4溶液的原因可能是__;铅与硝酸在酸溶过程中发生反应的离子方程式为__。
(3)流程中可循环利用的物质是__;洗涤操作时,检验沉淀是否洗涤干净需要的试剂是__。
(4)当沉淀转化达平衡时,滤液l中c(![]() )与c(
)与c(![]() )的比值为__。
)的比值为__。
(5)50~60℃时合成三盐的化学方程式为__;若得到纯净干燥的三盐99.0t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
物质 | 检验试剂 | 除杂试剂 |
(Ⅰ)甲烷(乙烯) | ________。 | ________。 |
(Ⅱ)酒精(水) | ________。 | ________。 |
①检验试剂:
A.无水硫酸铜 B.酸性高锰酸钾溶液
C.水 D.氢氧化钠溶液
②除杂试剂:
a.无水硫酸铜 b.乙酸
c.新制的生石灰 d.溴水
除杂时,乙烯发生反应的化学方程式为____________________。
(2)如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
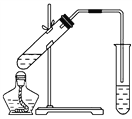
试回答:
在右试管中通常加入________溶液,实验生成的乙酸乙酯,其密度比水________,是有特殊香味的液体。分离右试管中所得乙酸乙酯的操作为(只填名称)________。反应中加入浓硫酸的作用是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体由两种气态烃组成,取标况下![]() 该混合气体完全燃烧后得到
该混合气体完全燃烧后得到![]() 二氧化碳
二氧化碳![]() 气体已折算为标准状况
气体已折算为标准状况![]() 和10.8g水,则这两种气体可能是
和10.8g水,则这两种气体可能是
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】压缩天然气汽车以天然气代替汽车用油,具有价格低、污染少、安全等优点。未经处理的天然气含有H2S,直接使用会造成大气污染,T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法错误的是( )
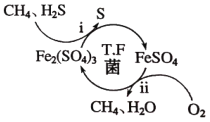
A.Fe2(SO4)3可以视为该脱硫过程中的催化剂
B.该脱硫过程的总反应为:2H2S+O2=2S+2H2O
C.该脱硫过程不能在高温下进行
D.该脱硫过程是将H2S转化为FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性介质中,H2O2能使 KMnO4溶液褪色,离子反应(未配平)为:MnO![]() + H+ + H2O2→Mn2++ O2 + H2O,下列说法错误的是
+ H+ + H2O2→Mn2++ O2 + H2O,下列说法错误的是
A.氧化性比较:MnO![]() > O2
> O2
B.该反应中酸性介质可以为盐酸
C.氧化剂与还原剂的物质的量之比为2∶5
D.若有0.1 mol氧化产物生成, 则转移电子0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工原料。
Ⅰ、某学习小组同学设计了下图所示的实验装置(部分夹持仪器未画出),进行氨气实验室制备且探究氨气的还原性及产物的检验。
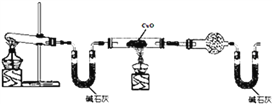
实验现象为:黑色CuO变为红色;干燥管中无水CuSO4粉末变为蓝色;同时生成一种无色无味无污染的气体。
(1)请写出大试管中反应的化学方程式_______________________________________。
(2)请写出氨气与CuO反应的化学方程式_________________________________________。
(3)该装置存在明显缺陷,请指出存在的问题______________________。
Ⅱ、哈伯因为将氮气和氢气在一定条件下合成氨气的成果面获得1918年诺贝尔化学奖。现将1molN2和3molH2充入一恒容的密闭容器中,使其在一定条件下达到平衡N2+3H2![]() 2NH3,下列哪些状态一定是达到平衡的状态?(_____)
2NH3,下列哪些状态一定是达到平衡的状态?(_____)
A.混合气体的平均相对分子质量不随时间改变而改变的状态
B.N2、H2、NH3的总物质的量不随时间改变而改变的状态
C.混合气体的密度不随时间改变而改变的状态
D.单位时间内0.1molNH3分解的同时,有0.05molN2生成的状态
Ⅲ、下图是一种电化学制备NH3的装置,图中陶瓷在高温时可以传输H+。
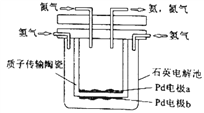
(1)H+经质子传输陶瓷由_____________流向_______________。(选填“a”或“b”)
(2)阴极发生的电极反应为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为
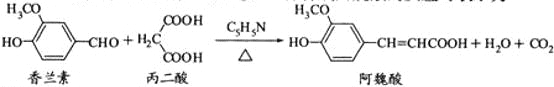
下列说法正确的是
A. 可用酸性![]() 溶液检测上述反应是否有阿魏酸生成
溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与![]() 、
、![]() 溶液反应
溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com