
【题目】下列物质按纯净物、胶体、电解质、氧化物的顺序组合的一组为( )
A. 稀盐酸、氨水、硫酸、干冰
B. 蒸馏水、淀粉溶液、碳酸氢钠、二氧化硫
C. 胆矾、雾、铁、石膏
D. 生石灰、泥水、氯化铜、碳酸钠
科目:高中化学 来源: 题型:
【题目】从镍矿石尾矿中提取NiSO4是解决我国镍资源匮乏的一条重要途径,已知该过程如下:
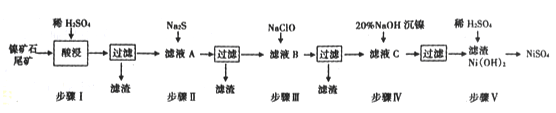
表1:各物质的Ksp数据如下表:
物质 | MnS | NiS | PbS | CuS | Ni(OH)2 |
Ksp | 2.5×10-13 | 1.1×10-21 | 8.0×10-28 | 6.3×10-36 | 2.0×10-15 |
表2:滤液A中各金属离子的含量如下表:
成分 | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | …… |
3.80 | 4.80 | x | 0. 20 | 0.15 | <0.001 | …… |
根据以上信息,回答下列问题:
(1)步骤I酸浸之前需将矿石粉碎,目的是____________。
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤Ⅱ中当Pb2+“恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=_____________
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ ClO - +5H2O=2Fe( OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式______________。
(4)为测定滤液A中Fe2+离子的含量,(每升溶液中含有的亚铁离子的质量,以g/L表示)每次移取20.00 mL待测液,并用0.02 mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18. 00mL,则x的值为________(精确到小数点后两位)。
(5)所得Ni(OH)2是制造镍镉电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH) +2H2O![]() Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
则随着放电的进行,正极区pH______(填“增大”、“减小”或“不变”);充电时阴极电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚对苯二甲酸乙二酯(J)具有良好的力学性能,其薄膜的伸拉强度是聚乙烯薄膜的9倍。它的合成路线如下:
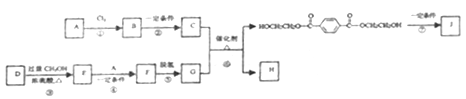
已知:
①![]()
②酯与醇可发生如下酯交换反应:RCOOR′+R〞OH ![]() RCOOR〞+R′OH(R、R′、R〞代表烃基)
RCOOR〞+R′OH(R、R′、R〞代表烃基)
(1)A的产量标志着一个国家石油化工发展水平,反应①的反应类型为______________。
(2)C的分子式是C2H6O2,是汽车防冻液的主要成分。反应②的试剂和反应条件是____________。
(3)D的分子式是C6H6O4,是一种直链结构的分子,核磁共振氢谱有3种峰,D种含有的官能团是______。
(4)F的结构简式是__________________。
(5)反应⑥的化学方程式是_________________。
(6)反应⑦为缩聚反应,反应⑦的化学方程式是_________________。
(7)G是一种同分异构体,G′为甲酸酯,核磁共振氢谱有3种峰且1mol该有机物酸性条件下水解产物能与2molNaOH反应。G′的结构简式为______________。
(8)以对二甲苯、甲醇为起始原料,选用必要的无机试剂合成G,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由相同条件下的三个反应:2A-+B2=2B-+A2 ;2C-+A2=2A-+C2 ;2B-+D2=2D-+B2可以判断正确的是( )
A.氧化性:A2>B2>C2>D2 B.还原性:A->B->C->D-
C.2A-+D2=2D-+A2反应可以进行 D.2C-+B2=2B-+C2反应不能进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是( )
A. Ba(OH)2溶液滴入稀硫酸中 B. 氢氧化钠溶液和稀硝酸反应
C. 氢氧化镁和稀盐酸反应 D. NaOH溶液滴入醋酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某单烯烃A(C8H16)可以发生如下图示的转化,回答下列问题

已知: ![]()

(1)B的分子式为____________,D中含有官能团的名称______________。
(2)B无银镜反应,D在浓硫酸存在下加热可得到能使溴水褪色且只有一种结构的物质E(不考虑立体异构),请写出E的结构简式____________________,D→E的反应类型_______________。
(3)写出C→F的化学方程式_________________。
(4)H的同分异构体中,满足下列要求的结构一共有____________种(不考虑立体异构,包括H本身)
①属于酯类;②酸性条件下水解能得到相对分子质量为74的有机物
(5)已知:
请写出由C制备2-丙醇的合成路线____________(无机原料任选)。合成路线流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁(Ⅲ)酸钾是制备负载活性催化剂的主要原料。加热至110℃时失去结晶水,230℃时分解。极易感光,室温下光照变为黄色:
2K3[Fe(C2O4)3]·3H2O![]() 2FeC2O4·2H2O+3K2C2O4+2CO2↑+2H2O
2FeC2O4·2H2O+3K2C2O4+2CO2↑+2H2O
已知:
物质名称 | 化学式 | 相对分子质量 | 颜色 | 溶解性 |
三草酸合铁(Ⅲ)酸钾 | K3[Fe(C2O4)3]·3H2O | 491 | 翠绿色 | 可溶于水,难溶于乙醇 |
草酸亚铁 | FeC2O4·2H2O | 180 | 黄色 | 难溶于水,可溶于酸 |
某同学对三草酸合铁(Ⅲ)酸钾的制备及组成进行了实验探究。回答下列问题:
(一)三草酸合铁(Ⅲ)酸钾的制备
(ⅰ)称取4.50 g FeC2O4·2H2O固体,加入饱和K2C2O4溶液中,用滴管慢慢加入3% H2O2溶液,不断搅拌,并保持温度在40℃左右。充分反应后,沉淀转化为氧氧化铁。
(ⅱ)加热至沸腾,滴加1mol 的草酸溶液至沉淀溶解。用草酸或草酸钾调节溶液pH=4-5
(ⅲ)小火加热浓缩,冷却结晶,过滤,先用少量冰水洗涤,再用无水乙醇洗涤,低温干燥后称量,得到9.80g 翠绿色晶体。
(1)完成步骤(i)发生反应的离子方程式:
____FeC2O4·2H2O+______C2O42-+____H2O2=___Fe(OH)3+4[Fe(C2O4)3]3-+____H2O
(2)步骤(ⅲ)中,用无水乙醇洗涤晶体的目的是________。
(3)列式计算本实验中三草酸合铁(Ⅲ)酸钾的产率______________。
(二)草酸根含量侧定
准确称取4.80g 三草酸合铁(Ⅲ)酸钾样品,配制成250mL 溶液。量取25.00 mL 溶液置于锥形瓶中,加入5.0 mL 1mol/L H2SO4,用0.06mol/L的KMnO4 溶液滴定。滴定终点时消耗KMnO4溶液20.00mL。
(4)滴定过程中,盛放高锰酸钾溶液的仪器名称是_______________,滴定时发生反应的离子方程式为_____。
(5)样品中草酸根的物质的量为_______;若该数值大于4.80g二草酸合铁(Ⅲ)酸钾纯品中草酸根的物质的量,其原因可能是_______(填字母)。
a.制取过程中草酸或草酸钾用量过多
b.样品未完全干燥
c.滴定时盛放KMnO4溶液的仪器未用标准液润洗
d.锥形瓶洗净后未烘干
(三)某同学制得的三草酸合铁(Ⅲ)酸钾,晶体表面发黄,推测可能有部分晶体发生了分解。
(6)为了验证此推测是否正确,可选用的试剂是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com