
【题目】铜锌原电池(如图)工作时,下列叙述错误的是( )

A. 正极反应为:Cu2++2e–= Cu
B. 电池反应为:Zn+Cu2+=Zn2+ +Cu
C. 在外电路中,电子从负极流向正极
D. 盐桥中的K+移向ZnSO4溶液
科目:高中化学 来源: 题型:
【题目】白色固体混合物A,含有KCl、CaCO3、Na2CO3、Na2SiO3、CuSO4中的几种,常温常压下进行如下实验。
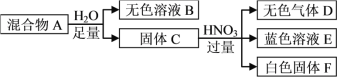
下列推断不正确的是
A. 无色溶液B的pH≥7
B. 白色固体F的主要成分是H2SiO3
C. 混合物A中有Na2SiO3、CuSO4和CaCO3
D. 在无色溶液B中加HNO3酸化,无沉淀;再滴加AgNO3,若有白色沉淀生成,说明混合物A中有KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各种矿产资源的开发利用为人类发展提供了重要的物质保障,如图是一些矿产资源的利用流程:
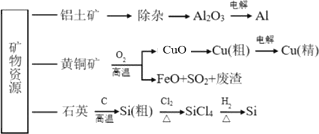
则下列说法不正确的是( )
A.铝热法也可以用来生成金属铝
B.黄铜矿中至少含有Cu、Fe、S三种元素
C.粗硅与氯气反应的目的是为了得到容易提纯的SiCl4
D.上述每种产品的生成过程都涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究SO2与Fe3+间是否发生氧化还原反应,按如图装置进行实验(夹持、加热仪器略),下列说法正确的是( )
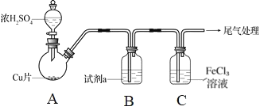
A.A中的反应仅体现了浓硫酸的氧化性
B.试剂a为饱和NaHCO3溶液
C.C中溶液pH降低,证明Fe3+氧化了SO2
D.检验C中的溶液含有Fe2+,证明Fe3+氧化了SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质检验是化学研究常用的方法之一。下列说法正确的是
A.若滴加硝酸银溶液,产生白色沉淀,则原溶液一定含Cl-
B.若滴加碳酸钠溶液,产生白色沉淀,则原溶液一定含Ca2+
C.若滴加硫氰化钾溶液,无明显变化,再滴入氯水溶液变红,则原溶液一定含Fe2+
D.若滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原溶液一定含CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是常见的有刺激性气味的硫氧化物,是大气主要污染物之一。某学习兴趣小组设计如下所示装置制取SO2并探究其性质。

(1)仪器a的名称是________,装置B中观察到的现象是________。
(2)装置C中氯水褪色,证明SO2具有________(填“氧化性”“还原性”或“漂白性”)。
(3)装置D中出现淡黄色沉淀,发生反应的化学方程式为________。
(4)某同学认为在A、B间应增加F装置,该装置的作用是________。
(5)装置E能否证明SO2是酸性氧化物________(填“能”或“不能”),理由是________。
(6)硫的氧化物是形成酸雨的主要物质之一。某小组采集酸雨样品,每隔一段时间测定一次样品pH,得数据如下:
时间 | 开始 | 8h | 16h | 24h | 32h | 40h | 48h |
pH | 5.0 | 4.8 | 4.6 | 4.3 | 4.2 | 4.0 | 4.0 |
酸雨样品pH变小的主要原因是________(用发生反应的化学方程式解释)。某同学在48h后偶然测得样品的pH又减小到3.9,导致样品pH再次减小的原因可能是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是我国化工专家侯德榜发明的联合制碱法简要流程:

关于此流程说法正确的是
A. 副产品Y是NH4HCO3B. 向母液中通入的气体X是CO2
C. 循环II是为了提高食盐的利用率D. 析出NaHCO3后的母液中只含NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学学科的一种重要学习手段,硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ.(查阅资料)
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.(产品制备)实验装置如图所示(省略夹持装置):
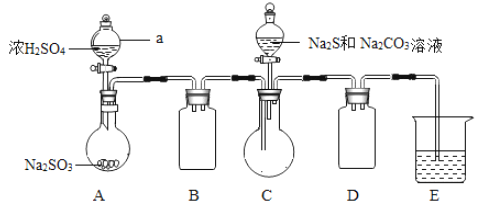
实验步骤:
(1)组装好仪器后,接下来应该进行的实验操作是______,仪器a的名称是______________;E中的试剂是____________(选填下列字母编号),作用是___________________。
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)按图示加入试剂。
(3)已知Na2S2O3·5H2O的溶解度随温度升高显著增大,待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合物,滤液经______(填操作方法)、冷却结晶、过滤、洗涤、干燥,得到产品,过滤时用到的玻璃仪器有_______________。
Ⅲ.(探究与反思)
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,是否说明一定有Na2SO4,__(填“是”或“否”),过滤,向白色沉淀中加入足量稀盐酸,如果产品中含有Na2SO3和Na2SO4,则加入稀盐酸产生的现象是______;
(2)为减少装置C中生成Na2SO4的量,应该先打开______(填“A”或“C”)装置上的活塞。
(3)所得粗产品可以通过_________________方法提纯(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A | B | C | D | |
实验 | 分离酒精和水 | 分离胶体和溶液 | 除去碳酸钠固体中的碳酸氢钠 | 比较碳酸钠和碳酸氢钠的稳定性 |
装置或仪器 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com