
【题目】下列关于乙醇在各种反应中断裂键的说法不正确的是( )
A.乙醇与钠反应,键①断裂
B.乙醇在Ag催化作用下与O2反应,键①③断裂
C.乙醇完全燃烧时,只有①②键断裂
D.乙醇、乙酸和浓硫酸共热制乙酸乙酯,键①断裂
科目:高中化学 来源: 题型:
【题目】肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4H2O+NaCl
实验一:制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是
;
实验二:制取水合肼(实验装置如图所示)控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充 分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分.(已知:N2H4H2O+2NaClO=N2↑+3H2O+2NaCl)
(2)分液漏斗中的溶液是(填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是
实验三:测定馏分中肼含量
水合肼具有还原性,可以生成氮气.测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250mL溶液.
b.移取25.00mL于锥形瓶中,加入10mL水,摇匀.
c.用0.2000mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右.记录消耗碘的标准液的体积.
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”);若本次滴定消耗碘的标准溶液为18.00mL,馏分中水合肼(N2H4H2O)的质量分数为(保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是: . 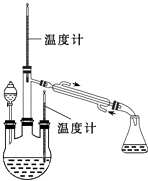
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙固体登山运动员常用的能源提供剂.某兴趣小组长拟选用如图装置制备氢化钙. 
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此判断,上述实验确有CaH2生成.
①写出CaH2与水反应的化学方程式;②该同学的判断不正确,原因是
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境已经成为人类的共识。人类应以可持续发展的方式使用资源,以合理的方式对废物进行处理并循环使用。下列做法不利于环境保护的是( )
A.发电场的煤脱硫处理
B.将煤转化为水煤气作燃料
C.回收并合理处理聚乙烯塑料废物
D.电镀废液经中和后直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题关系到人类的生存和发展,保护环境就是保护人类自己从保护环境的角度出发,目前最有发展前景的一次性餐具是 ( )
A.瓷器餐具
B.塑料餐具
C.淀粉餐具
D.不锈钢餐具
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.混合溶液的pH=7
B.混合溶液中,c(H+)= ![]() mol/L
mol/L
C.a=b
D.混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com