
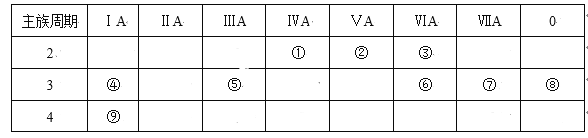
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_____(填具体化学用语,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______,碱性最强的化合物的电子式是:_____。
(3)最高价氧化物是两性氧化物的元素是___;写出它的氧化物与氢氧化钠反应的离子方程式__。
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:______。
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________。
(6)用结构式表示元素①与③形成的化合物____,该化合物在固体时俗称___,属于____晶体,指出它的一种用途___。
【答案】Ar HClO4 ![]() Al Al2O3+2OH-=2AlO2-+H2O 4NH3+5O2
Al Al2O3+2OH-=2AlO2-+H2O 4NH3+5O2![]() 4NO+6H2O或4NH3+3O2
4NO+6H2O或4NH3+3O2![]() 2N2+6H2O 3NO2+H2O=2HNO3+NO O=C=O 干冰 分子 人工降雨
2N2+6H2O 3NO2+H2O=2HNO3+NO O=C=O 干冰 分子 人工降雨
【解析】
由元素在周期表中的位置分析元素的种类,进而根据元素周期律及元素性质分析解答。
由元素在周期表中的位置可知,①为C,②为N,③为O,④为Na,⑤为Al,⑥为S,⑦为Cl,⑧为Ar,⑨为K,
(1)上述元素中,最不活泼的为稀有气体Ar,
故答案为:Ar;
(2)最高价氧化物的水化物中,酸性最强的化合物的分子式为HClO4;碱性最强的化合物为KOH,其电子式是![]() ,
,
故答案为:HClO4;![]() ;
;
(3)最高价氧化物是两性氧化物的元素是Al,其氧化物与氢氧化钠反应的化学方程式为Al2O3+2NaOH═2NaAlO2+H2O,离子方程式为:Al2O3+2OH-═2AlO2-+H2O;
故答案为:Al;Al2O3+2OH-═2AlO2-+H2O;
(4)②氢化物为氨气,③的单质为氧气,在一定条件下反应的化学方程式为4NH3+5O2![]() 4NO+6H2O或4NH3+3O2
4NO+6H2O或4NH3+3O2![]() 2N2+6H2O,
2N2+6H2O,
故答案为:4NH3+5O2![]() 4NO+6H2O或4NH3+3O2
4NO+6H2O或4NH3+3O2![]() 2N2+6H2O;
2N2+6H2O;
(5)②为N,红棕色气体为二氧化氮,可以与水反应,故不可以用排水法收集,方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
(6)用结构式表示元素①与③形成的化合物为二氧化碳,结构式为:O=C=O;该化合物在固体时俗称干冰;属于分子晶体;它的一种用途是人工降雨,
故答案为:O=C=O;干冰;分子;人工降雨。


科目:高中化学 来源: 题型:
【题目】“空气吹出法”海水提漠的工艺流程如下:

下列说法中,正确的是
A. 进入吹出塔前,Br -被还原成了Br2 B. 从吹出塔进入吸收塔的物质只有Br2
C. 经过吸收塔后,溴元素得到了富集 D. 蒸馏塔中只发生了物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 化学键的断裂和化学反应中能量变化的根本原因
B. 凡吸热反应均需在加热条件下才能发生
C. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
D. 因为石墨变成金刚石吸热,所以金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是( )
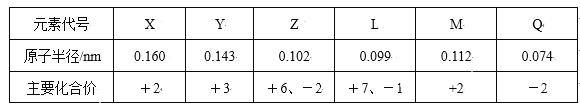
A. 等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多
B. Y与Q形成的化合物不可能跟氢氧化钠溶液反应
C. Z的氢化物的稳定性强于L的氢化物的稳定性
D. 与稀盐酸反应的剧烈程度:M单质<X单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______________,基态铜原子中,核外电子占据最高能层的符号是_________________,占据该最高能层的电子数为__________________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________(填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为______________。 (SCN)2对应的酸有硫氰酸(H-S-C![]() N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________。
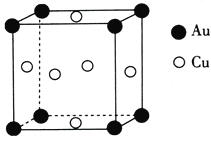
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____________(用含a、NA的代数式表示)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H1=-159.47kJ/mol K1
NH2COONH4(s) △H1=-159.47kJ/mol K1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3 K3
CO(NH2)2(s)+H2O(g) △H3 K3
请回答下列问题:
(1)①总反应的△H3=_______kJ/mol。该热化学方程式的平衡常数K3=____________(用K1、K2表示)。
②反应I一般在_________(填“高温”或“低温”)情况下有利于该反应的进行。
③一定温度下,在体积为固定的密闭容器中按计量比进行反应I,下列不能说明反应达到了平衡状态的是__________(填序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2)
D.容器内混合气体的密度不再变化
④环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)。
(2)在体积可变的恒压(p总)密闭容器中充入1 mol CO2 与足量的碳,让其发生反应:C(s)+ CO2(g)![]() 2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。

①T℃时,在容器中若充入稀有气体,v(正)___v(逆)(填“>”“<”或“=”);若充入等体积的CO2 和CO,平衡________移动(填“正向”“逆向”或“不”)。
②650℃,CO2 的转化率为_____________。
③已知:气体分压(P分)=气体总压×体积分数。用平衡分压代替平衡浓度表示平衡常数,925℃时,Kp=_____________ (用含P总的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图所示化合物的说法不正确的是

A. 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B. 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体。
C. 既可以催化加氢,又可以使酸性KMnO4溶液褪色
D. 1 mol该化合物最多可以与3 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100 mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度约为( )
A. 0.011 mol/L B. 0.22 mol/L C. 0.022 mol/L D. 0.11 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下列仪器和药品组成一套由含有硫化钙杂质的电石进行乙炔气体的制备、净化、检验,并可通过计算确定乙炔产率的系列实验装置,溴水的浓度为0.1 mol/L,体积是20mL,NaOH溶液足量。
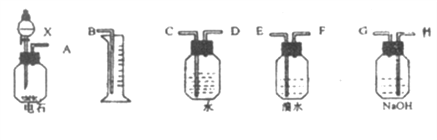
(1)如果所制气体从左到右流向时,进行实验时仪器的正确连接顺序是(填A、B、…) ____ 接 ; 接 ; 接 ; 接 。
(2)为了使实验中气流平稳,液体X通常用_________________________。
(3)实验中盛溴水的瓶中可观察到的现象是_________________________。
(4)假定溴水与乙炔完全反应,生成C2H2Br4,用含amol碳化钙的电石Wg与足量X反应,反应完全后,量筒内排入了VL液体(在标准状况下测定),则乙炔的产率为_____________________(只需列出算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com