
【题目】某同学设计如下元素周期表,已知X元素的气态氢化物水溶液呈碱性,空格中均有对应的元素填充。以下说法正确的是( )
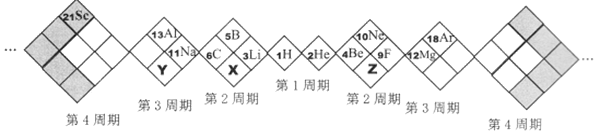
A. X、Y、Z元素分别为N、P、O
B. 白格中都是主族元素,灰格中都是副族元素
C. 因Y元素单质比X元素的单质活泼,故Y元素的非金属性比X要强。
D. X、Y、Z的气态氢化物中最稳定的是:X的氢化物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、E四种常见物质含有同一种元素,其中E是一种强酸,在一定条件下,它们有如图所示转化关系。下列推断不合理的是

A. X可能是一种氢化物
B. Y可能直接转化为E
C. Y不可能转化为X
D. 若X是单质,则X转化为Y的反应可能是化合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物W可用作高分子膨胀剂,一种合成路线如下:

回答下列问题:
(1)A的化学名称为________。
(2)②的反应类型是__________。
(3)反应④所需试剂,条件分别为________。
(4)G的分子式为________。
(5)W中含氧官能团的名称是____________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积比为1∶1)______________。
(7)苯乙酸苄酯( )是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
)是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产H的主要方法,E的溶液能发生银镜反应,G是具有香味的液体,试回答下列问题。
(1)F中所含官能团的名称是_____________________________________。
(2)G的结构简式为___________________________。
(3)写出D→E的化学方程式,并注明反应类型:____________________________。
(4)F→G的反应装置如图所示:

a.图中倒置球形干燥管的作用_____________________________;
b.试管Ⅱ中加有饱和Na2CO3溶液,其作用是: ____________________;
c.具有一个羟基的化合物M 10 g,与F反应生成产物11.85 g,并回收了未反应的M 1.3 g,则M的相对分子质量为____;
(5)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ,再测有机物层的厚度,实验记录如下:
实验编号 | 试管Ⅰ中试剂 | 试管II中试剂 | 有机层的厚度/cm |
A | 2ml乙醇、1ml乙酸、1ml18mol/L浓硫酸 | 饱和碳酸钠溶液 | 3.0 |
B | 2ml乙醇、1ml乙酸、 | 0.1 | |
C | 2ml乙醇、1ml乙酸、3ml 2mol/L硫酸 | 0.6 | |
D | 2ml乙醇、1ml乙酸、3ml 1mol/L硫酸 | 0.3 |
a.实验D与实验C相对照可证明___________________________________________________。
b.分析实验A、C的数据,可以推测出浓硫酸的__________提高了乙酸乙酯的产率。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④混合物中各物质的浓度不再变化
(7)写出G的一种同分异构体(与G同类)的结构简式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后溶液中有棕色、黑色现象出现。过一段时间后,发现经硫酸酸化的高锰酸钾溶液褪色。

甲同学认为酸性高锰酸钾溶液褪色,能证明乙烯被酸性高锰酸钾溶液氧化了;乙同学认为酸性高锰酸钾溶液褪色,不能证明乙烯被酸性高锰酸钾溶液氧化了。
(1)你认为哪个同学的观点正确? _____(填“甲”或“乙”),理由是_____ (填代号)。
A.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了氧化反应
B.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了加成反应
C.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,不能证明通入的气体是纯净物
D.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,只能证明通入的气体一定具有还原性
(2)丙同学取(Ⅱ)瓶中少量溶液于试管里,加入盐酸和氯化钡溶液,产生白色沉淀,他认为乙烯中一定混有二氧化硫,你认为他的结论是否可靠? _____(填“可靠”或“不可靠”);理由是_____________________。若你认为不可靠,改进上述实验方案,证明乙烯中是否含有SO2:__________________ 。
(3)丁同学对上述实验方案进行了适当改进,用于证明乙烯能否发生加成反应,他的改进方法可能是在装置(Ⅰ)和(Ⅱ)之间增加一个装有足量_____的洗气瓶且将(Ⅱ)瓶中溶液换成_____,发生反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)C在周期表中的位置____________________;
(2)由A、B、C三种元素形成的离子化合物的化学式为______________________。
(3)元素C、D、E形成的离子半径大小关系是___________________(用离子符号表示).
(4)用电子式表示化合物D2C的形成过程____________________________________。
C、D还可形成化合物D2C2,D2C2含有的化学键是_____________________________。其主要用途有______________________。
(5)现有空气中加热片刻生成的D的氧化物(假定全为D2C2和D2C的混合物)a克,与VLHCl反应至中性,则HCl的浓度取值范围为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 一定温度下,弱酸的电离常数越大,酸性越强
B. 醋酸的电离常数Ka和醋酸钠的水解常数Kh之间的关系为:Ka·Kh=Kw
C. 平衡常数只受温度影响,与反应物或生成物的浓度无关
D. 合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推理正确的是
A. 铝粉在氧气中燃烧生成Al2O3,铁丝在氧气中燃烧也生成Fe2O3
B. 铁能从硫酸铜溶液中置换出铜,钠也能从硫酸铜溶液中快速置换出铜
C. 铝片表面易形成致密的氧化膜,钠块表面也易形成致密的氧化膜
D. 钠与氧气、水等反应时钠均作还原剂,金属单质参与氧化还原反应时金属均作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com