
已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH) l.8 xl0-5,Ka(HSCN) 0.13
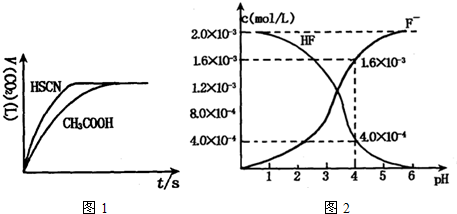
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图。
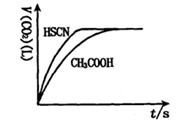
反应开始时,两种溶液产生CO2的速率明显不同的原因是 ;
反应结束后所得溶液中c(SCN-)____ c(CH3COO-)(填“>”,“=”或“<”)。
(2)2.0×l0-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如下图。
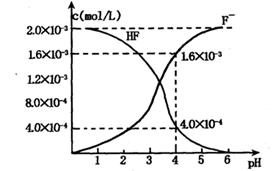
则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp= 1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4 mol/L的CaCl2溶液等体积混合,调节溶液pH =4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?____ (填“有”或“没有”),筒述理由: 。
(10分)(1)因为Ka(HSCN)>Ka(CH3COOH),溶液中c(H+):HSCN>CH3COOH, c(H+)大反应速率快(2分);> (2分)
(2)Ka(HF)=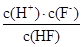 =
=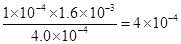 (2分)
(2分)
(3)有(2分)
因为溶液中c(Ca2+)·c2(F-)=5.12×10-10>ksp(CaF2)=1.5×10-10(2分)
【解析】
试题分析:(1)电离平衡常数大的电离出的离子浓度大,故反应开始时,两种溶液产生CO2的速率明显不同的原因是因为Ka(HSCN)>Ka(CH3COOH),溶液中c(H+):HSCN>CH3COOH,c(H+)大反应速率快。因为电离平衡常数不变,随着反应的进行,电离平衡正向移动,故c(SCN-)>c(CH3COO-)。
(2)电离平衡常数等于电离出的离子浓度的幂之积除以电解质的浓度,故Ka(HF)=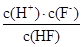 =
=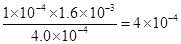 。
。
(3)查图可知当pH=4.0时,溶液中的c(F-)=1.6×10-3mol?L-1,因等体积混合则溶液中c(Ca2+)=2.0×10-4mol?L-1,即c(Ca2+)×c2(F-)=5.12×10-10>Ksp(CaF2))=1.5×10-10,所以有沉淀产生,故答案为:有沉淀产生。
考点:弱电解质在水溶液中的电离平衡 物质的量或浓度随时间的变化曲线 溶解平衡的计算
点评:本题考查电离平衡常数与弱电解质的电离、盐类水解的关系及利用溶度积来分析是否有沉淀生成,明确电离平衡常数的表达式和离子积的计算,并借助图来分析解答即可,较好的训练学生利用信息来分析问题、解决问题的能力。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省元氏一中高二上学期期中考试化学试卷(带解析) 题型:填空题
(8分)(1)已知25℃时弱电解质电离平衡常数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。25℃时,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为: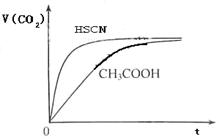
反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是 ,
反应结束后所得两溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)
(2)25℃时,将pH=1的H2SO4溶液a mL与pH=12的NaOH溶液b mL混合后,所得溶液的pH=3,则a:b= ;反应后,溶液中各离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源:2013届江西省南昌市高三上学期调研考试化学试卷(带解析) 题型:填空题
已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH) l.8 xl0-5,Ka(HSCN) 0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图。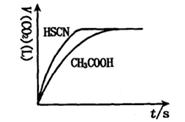
反应开始时,两种溶液产生CO2的速率明显不同的原因是 ;
反应结束后所得溶液中c(SCN-)____ c(CH3COO-)(填“>”,“=”或“<”)。
(2)2.0×l0-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如下图。
则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp= 1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4 mol/L的CaCl2溶液等体积混合,调节溶液pH =4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?____ (填“有”或“没有”),筒述理由: 。
查看答案和解析>>
科目:高中化学 来源:2013届河北省高二上学期期中考试化学试卷(解析版) 题型:填空题
(8分)(1)已知25℃时弱电解质电离平衡常数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。25℃时,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为:
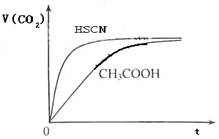
反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是 ,
反应结束后所得两溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)
(2)25℃时,将pH=1的H2SO4溶液a mL与pH=12的NaOH溶液b mL混合后,所得溶液的pH=3,则a:b= ;反应后,溶液中各离子浓度由大到小的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com