
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.l mol硫酸钾中阴离子所带电荷数为NA
B.乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有4NA个氢原子
C.22.4L氯气和足量氢气反应转移的电子数为2NA
D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.2NA个Cl-
【答案】B
【解析】
A、1mol硫酸钾中含有阴离子硫酸根离子的物质的量为1mol,1mol硫酸根离子带有2mol负电荷,所带电荷数为2NA,故A错误;
B、乙烯(C2H4)和环丙烷(C3H6)的实验式均为CH2,28g混合气体中含有CH2原子团的物质的量为![]() =2mol,含有4mol氢原子,所以28 g混合气体中含有4NA个氢原子,故B正确;
=2mol,含有4mol氢原子,所以28 g混合气体中含有4NA个氢原子,故B正确;
C、未告知温度和压强,气体摩尔体积不一定为22.4L/mol,无法计算22.4L氯气的物质的量,因此无法计算转移的电子数,故C错误;
D、氯化铁的化学式为FeCl3,将0.1mol氯化铁溶于1L水中完全电离,所得溶液含有Cl-0.3NA,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、Cl-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
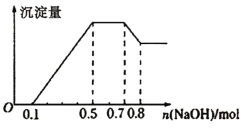
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中一定不含CO32-和SO42-,可能含有Cl-
C.溶液中n(Mg2+)=0.1mol
D.n(H+) :n(NH4+) : n(Al3+) : n(Mg2+)=2:4:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是几种常见有机物之间的转化关系图。A为常见医用消毒药品,C具有浓郁香味。
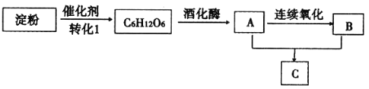
根据以上信息及各物质的转化关系,完成下列各题:
(1)A的结构简式为_____,写出工业上用乙烯生产A的化学方程式_________。
(2)B的官能团名称为______。
(3)A+B→C的化学方程式为______,反应类型为反应_______。
(4)下列说法正确的是_____
a.上图物质中只有C6H12O6属于糖类
b.转化1可在人体内完成
c.物质C属于油脂
d.物质A和B均为电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯时,经过配制混酸、硝化反应(50~60℃)、洗涤分离、干燥蒸馏等步骤,下列图示装置和原理能达到目的的
A. 配制混酸 B. 硝化反应
B. 硝化反应
C. 分离硝基苯 D. 蒸馏硝基苯
D. 蒸馏硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列信息合成含五元环有机化合物N的路线如图:
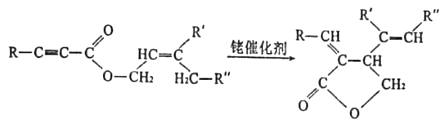
(R、R’、R”表示氢、烷基或芳基)
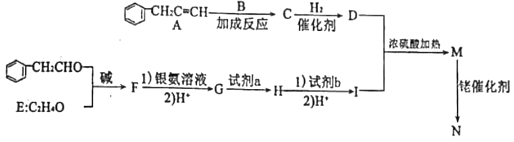
已知: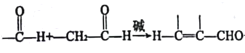 +H2O,B是E同系物,最大质荷比是30
+H2O,B是E同系物,最大质荷比是30
请回答下列问题:
(1)有机物A的系统命名___;
(2)C、D均为不饱和醇,D中含有官能团名称是___;
(3)设计实验,写出检验F中所含官能团的方法___;
(4)试剂a是___,H→I加入试剂b的反应方程式为___;
(5)写出满足下列条件G的所有(包含G)同分异构体有___种
①与G含有相同的官能团②苯环上最多有两个取代基
(6)写出N的结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL0.2 molL-1的稀硫酸。可供选用的仪器有:①托盘天平;②烧瓶;③烧杯;④药匙;⑤量筒;⑥玻璃棒。

(1)配制稀硫酸时,还缺少的仪器有________________(写仪器名称),
(2)下图是某些仪器的刻度部分示意图,其中为量筒的是________(填编号)。配制稀硫酸需要用量筒量取上述浓硫酸的体积为________mL,量取硫酸时应选用________(填选项)规格的量筒。
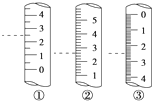
A.10mL B.50mL C.100mL D.200mL
(3)下图为量取浓硫酸后配制稀硫酸的操作示意图,其正确的操作步骤为_______(填编号)。
|
|
|
|
|
|
① | ② | ③ | ④ | ⑤ | ⑥ |
(4)对所配制的稀硫酸进行测定,发现其浓度大于0.2 mol/L,引起该误差的原因可能是_____。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
D.将稀释后的稀硫酸未冷却立即转入容量瓶后,紧接着就进行以后的实验操作
E.定容时,俯视容量瓶刻度线进行定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究苯和液溴的反应,设计了如下图所示实验装置进行。
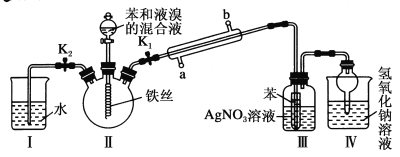
回答下列问题:
(1)冷凝管的进水口是________(填“a”或“b”)。
(2)关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。装置Ⅲ中小试管内苯的作用是______________。
(3)该实验能否证明苯和液溴发生了取代反应?_____(填“能”或“不能”),理由是______。
(4)反应结束后,关闭K1和分液漏斗活塞,打开K2,此时装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是_____________。
(5)最后将三颈烧瓶内的液体依次进行下列实验操作就可得到较纯净的溴苯。
a.用蒸馏水洗涤,振荡,分液;
b.用5%的NaOH溶液洗涤,振荡,分液;
c.用蒸馏水洗涤,振荡,分液;
d.加入无水CaCl2粉末干燥;
e.________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL1.5 mol/L的氢氧化钠溶液中缓慢通入一定量的CO2,反应后,向所得溶液中逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。下列说法错误的是
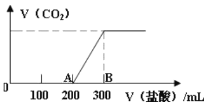
A.氢氧化钠溶液与一定量的CO2充分反应后的溶液中溶质为Na2CO3和NaHCO3
B.盐酸的浓度为0.5 mol/L
C.B点产生的气体在标准状况下体积1.12 L
D.AB段发生反应的离子方程式为:HCO3- + H+ = H2O+ CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
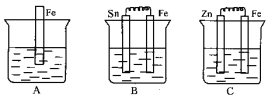
(1)A中反应的离子方程式为_________________________________。
(2)B中Fe极为_______极,电极反应式为_______________________。C中Fe极为_______极,电极反应式为__________________________,电子从_______极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com