
【题目】下列说法正确的是( )
A.有氧气参加的反应一定是燃烧
B.燃烧一定要有氧气参加
C.氢气在氯气中燃烧,火焰呈绿色
D.任何发光放热的剧烈的化学反应都可以叫燃烧
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如果1mol金刚石的质量为a g,密度为ρg·cm﹣3,请计算出每个碳原子的共价半径________(两个原子核之间距离的一半)(设碳原子为紧密堆积结构,见图)。(用含a,ρ,NA的式子表示。NA表示阿伏加德罗常数的值)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O﹣Cu2+﹣H2O轴线垂直).请回答以下问题:
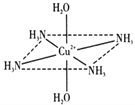
(1)硫酸铜水溶液加氨水的变化过程,用离子方程式表示为生成深蓝色溶液:__________.
(2)此深蓝色的离子中Cu2+与H2O和NH3形成的是________键,请在图中表示此化学键________.此深蓝色离子的空间结构呈________形.
(二).由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。如:Na2O+Cl2=2NaCl+O2、CaO+Cl2=CaCl2+O2、SiO2+2CCl4=SiCl4+2COCl2、Cr2O3+3CCl4=2CrCl3+3COCl2。请回答下列问题:
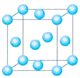
⑴与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有______(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为_____。
(2)COCl2俗称光气,分子中C原子采取sp2杂化成键,其中碳氧原子之间共价键是____(填序号)
a.2个σ键 b.2个π键 c.1个σ键、1个π键
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_________。CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO-3401kJmol-1、NaCl-786kJmol-1。导致两者晶格能差异的主要原因是_____________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了验证苯酚、醋酸和碳酸的酸性强弱,设计了如图所示实验装置。
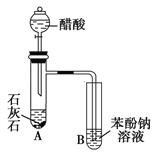
请回答下列问题:
(1)仪器B中的实验现象:____________________________________________。
(2)仪器B中发生反应的化学方程式是___________________________。
(3)该实验设计不严密,请改正:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。
![]()
已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________。
(2)丙、丁可形成AB2型化合物,其化学式为________。
(3)丙是自然界中形成化合物种类最多的元素,则丙是________(填名称),其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是________(填元素符号),写出这些化合物中任意两种符合以下条件的化学式______________________
(①原子个数比为1∶2;②分子中价电子总数为偶数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某有机物分子的球棍模型,该有机物中含C、H、O、N四种元素。下列关于该有机物的说法中错误的是
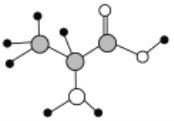
A. 分子式为C3H7O2N
B. 该有机物只能与NaOH溶液反应,不能与盐酸反应
C. 能通过聚合反应生成高分子化合物
D. 其同分异构体中有物质既不能与NaOH溶液反应,又不能与盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种不溶于水的固体非金属氧化物,根据图中的转化关系,回答下列问题:
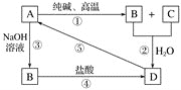
(1)写出化学式:A是____________,D是____________。
(2)写出相关反应的化学方程式:①____________,⑤____________。
(3)写出相关反应的离子方程式:②__________,③__________,④__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) ① 25℃时,NH4Cl溶液呈酸性,原因是______水解引起的(填“NH4+”或“Cl-”);
② 常温下,0.0100mol/L NaOH溶液的pH=___________;
③ 用0.0100mol/L 盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为_______(填“蓝色”或“无色”),且半分钟内颜色保持不变。
④ 已知在25℃:AgCl(s) ![]() Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag2S(s) ![]() 2Ag+(aq)+S2-(aq) Ksp=6.3×10-50
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50
向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是_________(填“AgCl”或“Ag2S”)。
(2)已知25℃合成氨反应中,1mol N2完全转化为NH3时释放的能量为92.4 kJ。现将1mol N2和3mol H2混合置于2L密闭容器中,反应进行到2s末测得NH3为0.4mol。
回答下列:
① 该反应的热化学方程式是______________ ;
② 该反应达到平衡后,升高温度平衡向_______ (填“正”、“逆”)反应方向移动;加入催化剂平衡________(填“正”、“逆”、 “不”)移动;
③ 前2s内v(H2)是___________。
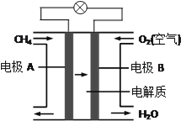
(3)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是 ________(填化学式);如果该电池中的电解质溶液是KOH溶液,电极B电极上发生的电极反应式是:______________。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)Ⅰ.化学课上老师演示了如下图的实验:
实验时,将两气球内的NaHCO3和Na2CO3同时倒入试管中。已知盐酸是足量的,且整套装置气密性良好,回答下列问题:
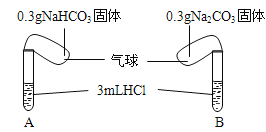
(1)实验过程中观察到的现象是:________________.
(2)实验结束后,两试管的气球大小有差异,大小气球(包含试管)体积之比约为(填最简单整数比)__________.
Ⅱ.当甲同学用手触摸上述试管时,意外发现A试管变冷,而B试管发热,他把这个发现告诉了同桌乙同学,并由此得出结论:NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.乙同学却对此结论却持怀疑的态度.为此,两位同学在课外活动中继续进行了下列实验(每次实验各做3次平行实验,取平均值):
序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后温度 |
① | 35mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
② | 35mL水 | 3.2g Na2CO3固体 | 20℃ | 24.3℃ |
③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10mL水 | 20℃ | 24.2℃ |
⑤ | 35mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
⑥ | 35mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
请你帮助填写相关内容:
(1)该研究报告的题目是《___________________________》.
(2)该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称是______________________.
(3)实验①和②的目的是_________________________________________________.
(4)通过上述实验可得出的结论是:___________________________________(写出两条即可).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com