
【题目】为了检验淀粉的水解产物,某学生设计了如下实验方案:
![]()
请回答下列问题
(1)试剂1为20%的H2SO4溶液,其作用是___________________;
(2)试剂2为_____,其作用是____________;
(3)反应①的化学方程式为_______________________;
(4)为了检验淀粉是否已经完全水解,取少量水解液于试管中,加入碘水。则证明淀粉未完全水解的现象是_____________。
【答案】作催化剂 NaOH溶液 中和作催化剂的硫酸,使检验水解产物的实验得以顺利进行;H+ +OH- ═H2O (C6H10O5)n+nH2O ![]() nC6H12O6 溶液变蓝
nC6H12O6 溶液变蓝
【解析】
(1)因淀粉水解需要催化剂,所以20%的H2SO4溶液作催化剂,故答案为:作催化剂;
(2)因淀粉水解用稀硫酸催化剂,检验葡萄糖时溶液要呈碱性,故要加氢氧化钠溶液中和硫酸,答案为:NaOH溶液;中和作催化剂的硫酸,使检验水解产物的实验得以顺利进行,离子反应为H+ +OH- ═H2O;
(3)反应①为淀粉的水解,化学方程式为:(C6H10O5)n+nH2O ![]() nC6H12O6 ;
nC6H12O6 ;
(4)因淀粉未完全水解时还有淀粉分子存在,而碘能使淀粉变蓝,故答案为:溶液变蓝。


科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是( )
A.烟、云、雾都属于胶体
B.硫酸钡、醋酸都属于弱电解质
C.SO2、NO2、CO 均为酸性氧化物
D.溶液与胶体的本质区别是溶液不能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列叙述是可逆反应N2(g)+3H2(g)![]() 2NH3(g),在定容密闭容器中达到平衡的标志的是 ( )
2NH3(g),在定容密闭容器中达到平衡的标志的是 ( )
①NH3的生成速率与NH3的分解速率相等;
②单位时间内amolN2生成,同时生成3amolH2;
③N2的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦N2、H2、NH3的分子数目比为1:3:2;
A.②⑤ B.①③④⑤ C.②⑥⑦ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有科学家正在研究用碳与一氧化氮反应处理环境问题
C(s)+2NO(g)![]() CO2(g)+N2(g)△H
CO2(g)+N2(g)△H
(1)实验方案中有下列措施:①采用加热提高反应速率,②使用催化剂提高反应速率,③使用加压提高NO转化率,④使CO2转化成干冰从体系用脱离,提高NO的转化率,你认为可行的是_________。
(2)这个反应的平衡常数表达式是_________________;
(3)在恒容恒温密闭容器中,科学家得到下列实验数据
时间(min) | 浓度(mol/L) | ||
NO | N2 | CO2 | |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
反应在该温度下的平衡常数K=_________________;
(4)若在(3)的实验中30min时开始升温,36min时达平衡,测得NO的转化率变为50%,则该反应的△H_______0(填“>”、“<”、“=”),判断的理由是___________________;
(5)若科学家在30min后改变了某一条件,反应进行到40min时达平衡浓度分别为c(NO)=0.032mol/L,c(N2)=0.034mol/L,c(CO2)=0.017mol/L,则改变的条件可能是______,判断的依据是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素随着原子核电荷数的增加,下列叙述不正确的是
A.原子半径依次增大B.单质的熔沸点逐渐升高
C.卤离子的还原性逐渐减弱D.氢化物的热稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃的混和物共0.1mol,完全燃烧后得3.36L(标况下)CO2和3.6g水,下列说法正确的是( )
A. 一定有乙烯B. 一定有甲烷
C. 可能有乙烷D. 一定有乙烷,但不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是
是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是
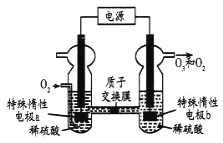
A. 电极a为阴极
B. 标准状况下,当![]() 反应时收集到
反应时收集到![]() 和
和![]() 混合气体
混合气体![]() ,
,![]() 的体积分数为80%
的体积分数为80%
C. 电解一段时间后b极周围的![]() 下降
下降
D. a极的电极反应为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖尿病是由于人体内胰岛素紊乱导致的代谢紊乱综合征,以高血糖为主要标志。长期摄入高热量食品或缺少运动,都会导致糖尿病。
(1)血糖是指血液中的葡萄糖,下列有关说法正确的是______________。
A.葡萄糖分子可表示为C6(H2O)6,则每个葡萄糖分子含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.糖尿病人尿糖较高,可用新制的氢氧化铜来检测人尿液中的葡萄糖
D.淀粉水解的最终产物是氨基酸
(2)糖尿病人不可过量饮酒,将会一定程度上造成胰岛细胞损伤。但酒精在肝脏内可转化成有机物A。A的实验结果如下:
①通过实验测得A的相对分子质量为60;
②A由C、H、O三种元素组成,分子中只存在两种类型的氢原子,且这两种类型的氢原子个数比为1∶3
③A可与酒精在一定条件下生成有芳香气味的物质。
纯净的A又称为______________,结构简式为____________________。
A的主要化学性质有(用化学方程式表示):a____________________________________,
b___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法是化学常用来定量测定物质浓度的一种重要的实验方法。在食品工业、药品制造、化妆品行业等等都被广泛应用。中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用如图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
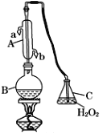
(1)仪器A的名称是________,水通入A的进口为________。B中加入300.00 mL葡萄酒和适量盐酸,加热B使SO2全部逸出并与C中H2O2完全反应。
(2)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为________。滴定终点现象为_______________。
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________g·L-1。
(4)该测定结果往往比实际值偏高,最可能的原因是_________________,在不改变装置的情况下,如何改进:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com