
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图:
回答下列问题:
(1)从反应开始到10s时,用Z表示的反应速率为_______, X的物质的量浓度减少了___________,Y的转化率为______________。
(2)该反应的化学方程式为_________________________。
(3) 10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是______________。
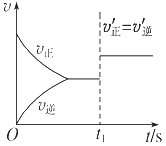
A.t1时刻,增大了X的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
【答案】 0.079mol/(Ls) 0.395mol/L 79.0% X(g)+Y(g)![]() 2Z(g) CD
2Z(g) CD
【解析】本题考查化学反应速率的计算以及影响化学平衡移动的因素,(1)根据化学反应速率数学表达式,v(Z)=1.58/(2×10)mol/(L·s)=0.079mol/(L·s);X减少的浓度为(1.2-0.41)/2mol·L-1=0.395mol·L-1,Y的转化率为(1-0.21)/1×100%=79.0%;(2)同一容器中,化学反应速率之比等于化学计量数之比等于物质的量变化之比,因此X、Y、Z的系数之比为:(1.2-0.41):(1-0.21):1.58=1:1:2,因此化学反应方程式为:X(g)+Y(g)![]() 2Z(g);(3)根据图像,t1时刻化学反应速率增大,但化学平衡不移动,A、增大X浓度,平衡向正反应方向移动,故A错误;B、升高温度,化学平衡必然改变,故B错误;C、缩小容器的体积,相当于增大压强,因为反应前后气体系数之和相等,因此增大压强,平衡不移动,但正逆反应速率增大,故C正确;D、使用催化剂加快反应速率,但平衡不移动,故D正确。
2Z(g);(3)根据图像,t1时刻化学反应速率增大,但化学平衡不移动,A、增大X浓度,平衡向正反应方向移动,故A错误;B、升高温度,化学平衡必然改变,故B错误;C、缩小容器的体积,相当于增大压强,因为反应前后气体系数之和相等,因此增大压强,平衡不移动,但正逆反应速率增大,故C正确;D、使用催化剂加快反应速率,但平衡不移动,故D正确。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】为探究某矿石(仅含两种元素)的组成和性质,设计并完成如下实验:
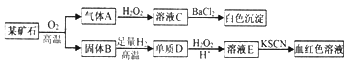
请回答:(1)某矿石的组成元素为__________(用元素符号表示)。
(2)气体A与H2O2溶液反应的化学方程式是________________。
(3)写出D→E的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,粒子的物质的量浓度关系正确的是( )
A. 向醋酸钠溶液中加入适量醋酸得到酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B. 0.1 mol·L-1NH4Cl溶液:c(NH![]() )=c(Cl-)
)=c(Cl-)
C. 0.1 mol·L-1Na2CO3溶液:c(OH-)=c(H+)+c(HCO![]() )+2c(H2CO3)
)+2c(H2CO3)
D. 向硝酸钠溶液中滴加稀盐酸得到pH=5的溶液:c(Na+)=c(NO![]() )+c(Cl-)
)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室现有一瓶标签右半部分已被腐蚀的固体M,剩余部分只看到“Na2S”字样(如图所示)。已知固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种。若取少量固体M配成稀溶液进行下列有关实验,其中说法正确的是( )

A. 往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3
B. 往溶液中加入稀盐酸酸化的BaCl2,若有白色沉淀,则固体M为Na2SO4
C. 用pH试纸检验,若pH=7,则固体M不一定是Na2SO4
D. 只用盐酸一种试剂不能确定该固体M的具体成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列两种溶液的说法中,正确的是( )
溶液①:0.2 mol·L-1CH3COONa溶液;溶液②:0.1 mol·L-1H2SO4溶液
A. 相同温度下,溶液中水的电离程度:溶液①<溶液②
B. 加水稀释溶液①,溶液中![]() 变大
变大
C. 等体积混合溶液①和溶液②,所得溶液中c(CH3COO-)+2c(SO![]() )=c(Na+)
)=c(Na+)
D. 25℃时,向溶液②中滴加溶液①至pH=7,溶液中c(Na+)>c(SO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能量转化过程与氧化还原反应无关的是
A. 硅太阳能电池工作时,光能转化成电能
B. 锂离子电池放电时,化学能转化成电能
C. 电解质溶液导电时,电能转化成化学能
D. 葡萄糖为人类生命活动提供能量时,化学能转化成热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知;还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和和析出的I2的物质的量的关系曲线如图。下列说法正确的是()

A.反应过程中的氧化产物均为Na2SO4
B.a 点时消耗NaHSO3的物质的量为1.0mol
C.0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
D.当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为1.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是( )
A. Na+ H+ NO3- Fe2+ B. Ca2+ H+ ClO- NO3-
C. K+ H+ Cl- SO42- D. Fe3+ Cl- H+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)除去自来水中的Ca2+、Mg2+、Cl—、SO42—等杂质,选择装置_____________(填代表装置图的字母)。
(2)用CCl4萃取碘水中的I2,有机层的颜色为___________________。
(3)装置A中①的名称是_____________,进水的方向是_____________。装置B在分液时为使液体顺利滴下,应进行的具体操作是_____________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。
正确的操作顺序是_____________(填写字母)。
a.⑤②③①⑥④⑦b.⑤①②③⑥④⑦ c.⑤③②①⑥④⑦d.⑤②①③④⑥⑦
问题2:由海水到氯化钠晶体的实验过程中要用到的主要装置是_____________(从给定的四种装置中选择,填字母)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com