
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是( )
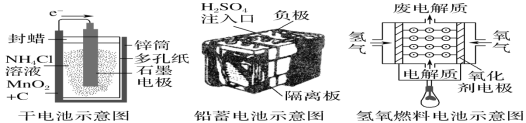
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池工作过程中,正、负电极质量均减轻
D.氢氧燃料电池是一种具有广阔应用前景的绿色电源
【答案】C
【解析】
干电池中,锌筒为负极,碳棒为正极,只能放电,不能充电。铅蓄电池放电时,Pb棒为负极,Pb失电子后转化成PbSO4附着在负极Pb表面;正极PbO2得电子产物与电解质反应生成PbSO4附着在PbO2表面。若接通直流电源,可进行充电。氢氧燃料电池中,通氢气的电极为负极,通氧气的电极为正极。
A.干电池属于一次电池,铅蓄电池属于二次电池,A正确;
B.干电池在长时间使用后,负极锌不断溶解,从而造成锌筒不断被破坏,B正确;
C.铅蓄电池工作过程中,正、负电极都转化为PbSO4,电极质量均增重,C不正确;
D.氢氧燃料电池产生的能量高,电池产物为水,是前景广阔的绿色电源,D正确;
故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4),也称为保险粉,Na2S2O4易溶于水,难溶于乙醇,具有极强的还原性,易被空气氧化,在碱性介质中稳定。其阴离子的结构如图所示: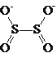 。某科研小组制备并探究其性质。
。某科研小组制备并探究其性质。
Ⅰ.制备Na2S2O4(加热等辅助仪器略去)
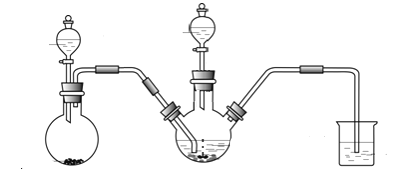
(1)Na2S2O4中硫元素的化合价为_______。
(2)连接好装置后,检查其气密性良好的操作是____________________。
(3)添加药品、再次连接好装置:
①第一步,将A中生成的气体通往B中进行反应,在B装置生成连二亚硫酸锌的化合反应方程式为__________;
②第二步,加入NaOH溶液,于28~35℃下反应生成Na2S2O4,该步反应的离子方程式为_____________。
第三步,将第二步的混合物过滤,并向滤液中加入固体NaCl,冷却至20℃,便有Na2S2O4晶体析出。
③第四步,将第三步所得混合物经________(填操作名称)、________(填写 “水”或“乙醇”)洗涤,得到纯净的Na2S2O4晶体。
(4)装置C的作用是 _______________。
Ⅱ.探究Na2S2O4的稳定性
(5)隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3和SO2,但科研小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______________。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )
![]()
A. N4分子的键角为109°28′B. N4的沸点比N2低
C. 1 mol N4分子所含共价键数为4NAD. N4分子中只含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸银(AgBrO3)和KNO3的溶解度随温度变化曲线如图所示:


下列分析错误的是( )
A.60℃时,AgBrO3,饱和溶液的浓度是0.596%
B.温度升高时AgBrO3,和KNO3溶解速度都加快
C.温度对AgBrO3,溶解度的影响比对KNO3溶解度的影响大
D.KNO3中少量AgBrO3可用重结晶的方法除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质在高空大气层中保护人类免遭太阳光中紫外线的强烈侵袭;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态价电子排布式可表示为_____。
(2)MX3-的空间构型是_________;H2X分子的空间构型为__________。
(3)从核外电子排布角度解释高温下Z2O比ZO更稳定的原因_________。
(4)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃,其晶胞结构如图所示。
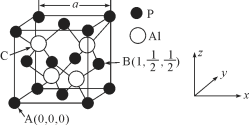
①磷化铝的晶体类型为_____。
②A、B点的原子坐标如图所示,则C点的原子坐标为____。
③磷化铝的晶胞参数a=546.35pm(1pm=10-12m),其密度为_____g/cm3(列出计算式即可,用NA表示阿伏加德罗常数的数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ:(1)将钠、铁、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:____________与盐酸反应最剧烈。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____________________________。
Ⅱ:利用如图装置可验证同主族元素非金属性的变化规律。

(1)仪器B的名称为_____________,干燥管D的作用为防止______________________。
(2)若要证明非金属性:Cl>I-,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下反应生成氯气,C中加淀粉-碘化钾混合溶液,观察到C中溶液__________________(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____________溶液吸收尾气。
(3)若要证明非金属性:![]() ,则在A中加盐酸、B中加
,则在A中加盐酸、B中加![]() 、C中加
、C中加![]() 溶液。观察到C中溶液_____________
溶液。观察到C中溶液_____________![]() 填现象
填现象![]() ,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有____________溶液的洗气瓶除去。
,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有____________溶液的洗气瓶除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A CH2 =CH—COOH和油酸(C17 H33COOH) B 12C60和石墨 C ![]() 和
和 ![]() D 35Cl和37Cl
D 35Cl和37Cl
①互为同位素的是________________;
②互为同系物的是_________________;
③互为同素异形体的是_____________;
④互为同分异构体的是_____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子共存的说法或离子方程式的书写中,正确的一组是( )
①加入NaOH溶液后的溶液中能大量共存的离子:NH4+、Al3+、SO42-
②pH=1的溶液中能大量共存的离子:Fe3+、Mg2+、Cl-、SO42-
③能使酚酞溶液变红的溶液中能大量共存的离子:K+、CO32-、Na+、S2-
④向 NH4HCO3溶液中加入足量NaOH溶液并共热:NH4++OH-=NH3↑+H2O
⑤用食醋溶解水垢:CaCO3+2H+=Ca2+ + CO2↑ + H2O
⑥向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
⑦用FeCl3溶液腐蚀铜电路板:2Fe3++Cu=2Fe2++Cu2+
A.①③⑤⑦B.②③⑥⑦C.②④⑤⑦D.③④⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com