
【题目】以有机物A(含有苯环的烃,化学式C8H8)和CCl4为原料合成苯丙氨酸E的流程如下:
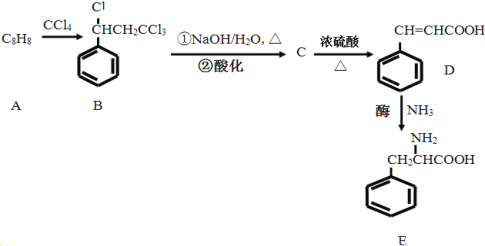
已知:烃分子中的氢原子被卤素原子取代所生成的衍生物叫做卤代烃,如CH3CH2Cl;卤代烃在NaOH水溶液加热条件下会水解,如:
CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl
CH3CH2OH+NaCl
CH2ClCH2Cl+2NaOH![]() CH2OHCH2OH+2NaCl
CH2OHCH2OH+2NaCl
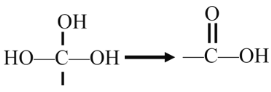 (该反应不需要条件就迅速转化)
(该反应不需要条件就迅速转化)
R-CH2CH2OH![]() R-CH=CH2+H2O
R-CH=CH2+H2O
(1)D→E的反应类型为_____________________。
(2)A的结构简式为________________________。
(3)有关D的叙述错误的是___________(填序号)。
a.能使酸性KMnO4溶液褪色 b.能与溴的CCl4溶液反应
c.能与甲醇发生酯化反应 d.能发生水解反应
(4)C→D反应的化学方程式为___________________________________。
(5)满足下列条件的E的同分异构体共有_________种。
①属于酯类;②苯环上只有两个对位取代基,其中一个为—NH2。
【答案】加成反应![]() d
d 6
6
【解析】
根据B结构简式知,A为![]() ,A发生加成反应生成B,B发生水解反应,然后酸化得到C,结合题给信息知,C结构简式为
,A发生加成反应生成B,B发生水解反应,然后酸化得到C,结合题给信息知,C结构简式为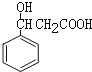 ,C发生消去反应生成D,D发生加成反应生成E,据此分析解答。
,C发生消去反应生成D,D发生加成反应生成E,据此分析解答。
根据B结构简式知,A为![]() ,A发生加成反应生成B,B发生水解反应,然后酸化得到C,结合题给信息知,C结构简式为
,A发生加成反应生成B,B发生水解反应,然后酸化得到C,结合题给信息知,C结构简式为 ,C发生消去反应生成D,D发生加成反应生成E;
,C发生消去反应生成D,D发生加成反应生成E;
(1)根据以上分析知,D发生加成反应生成E,反应类型是加成反应;正确答案:加成反应。
(2)通过以上分析知,A的结构简式为![]() ;正确答案:
;正确答案:![]() 。
。
(3)D中含有羧基、碳碳双键和苯环;据此分析如下:
a.含有碳碳双键,所以能被酸性高锰酸钾溶液氧化而使酸性KMnO4溶液褪色,故正确;
b.含有碳碳双键,所以能与溴的CCl4溶液反应而使溴的四氯化碳溶液褪色,故正确;
c.含有羧基,所以能与甲醇发生酯化反应,故正确;
d.不含卤原子或酯基,所以不能发生水解反应,故错误;
正确选项d;
(4)C发生消去反应生成D,反应方程式为:
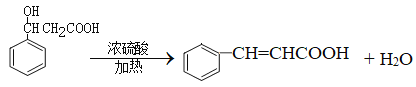 ;正确答案:
;正确答案: 。
。
(5)E的同分异构体符合下列条件:①属于酯类,说明含有酯基;②苯环上有两个对位取代基,其中一个为一NH2,则另一个为酯基,可能的结构有:HCOOCH2CH2- 、 HCOOCH(CH3)- 、CH3COOCH2- 、CH3CH2COO- 、CH3OOCCH2- 、CH3CH2OOC-6种结构;所以符合条件的有6种结构;正确答案:6。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】已知高能锂离子电池的总反应式为2Li+FeS=Fe+Li2S,LiPF6·SO(CH3)2为电解质,用该电池为电源电解含镍酸性废水并得到单质Ni的实验装置如图所示。下列说法不正确的是

A. 电极Y为Li
B. 电解过程中,b中NaCl溶液的物质的量浓度将不断减小
C. X极反应式为FeS+2Li++2e-=Fe+Li2S
D. 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国最新战机歼一31使用了高强度、耐高温的钛合金材料。工业上冶炼钛的反应为TiCl4+2Mg=Ti+2MgCl2。下列有关该反应的说法正确的是( )
A.Mg被氧化B.TiCl4是还原剂
C.Ti是氧化产物D.24g Mg参加反应转移1mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A. 摩尔是一个基本物理量
B. 1mol H2O中所含氧原子的质量为16g
C. 10L氢气比8L氢气所含H2的物质的量多
D. 某物质含有6.02×1023个粒子,则该物质的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学己经渗透到人类生活的方方面面。下列说法不正确的是
A. 为加快漂白精的漂白速率,使用时可滴加几滴醋酸
B. 明矾![]() 溶于水会形成胶体,因此可用于自来水的杀菌消毒
溶于水会形成胶体,因此可用于自来水的杀菌消毒
C. 月饼因富含油脂而易发生氧化,保存时常放入装有铁粉的透气袋作抗氧化剂
D. 为增强治疗缺铁性贫血效果,可在口服硫酸亚铁片时同服维生素C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为![]() 和
和![]() 反应生成
反应生成![]() 过程中的能量变化:下列说法中正确的是
过程中的能量变化:下列说法中正确的是
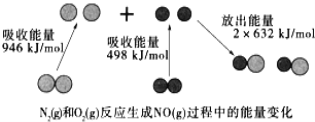
A. 1mol![]() 和1mol
和1mol![]() 完全反应吸收的能量为180kJ
完全反应吸收的能量为180kJ
B. 放电情况下,![]() 和
和![]() 混合能直接生成NO2
混合能直接生成NO2
C. 1mol![]() 和
和![]() 具有的总能量高于
具有的总能量高于![]() 具有的总能量
具有的总能量
D. NO是一种红棕色气体,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:![]() 已知该反应的速率随
已知该反应的速率随![]() 的增大而加快
的增大而加快![]() 为
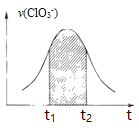
为![]() 的速率时间关系图。下列说法中正确的是
的速率时间关系图。下列说法中正确的是
A. 反应开始时速率增大一定是温度升高所致
B. 纵坐标为![]() 的
的![]() 曲线与图中曲线不重合
曲线与图中曲线不重合
C. 图中阴影部分的面积表示![]() 时间内
时间内![]() 的减小
的减小
D. 后期反应速率下降的主要原因是反应物浓度减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:

Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知:![]() )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。

(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com