
ЎҫМвДҝЎҝТСЦӘ°ұҝЙТФУлЧЖИИөДСх»ҜНӯ·ҙУҰөГөҪөӘЖшәНҪрКфНӯЈ¬УГКҫТвНјЦРөДЧ°ЦГҝЙТФКөПЦёГ·ҙУҰЎЈ

»ШҙрПВБРОКМвЈә
ЈЁ1Ј©AЦРјУИлөДОпЦККЗ_____________ўЩ_____________________________.
·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪКЗ_______________ўЪ_______________________;
ЈЁ2Ј©BЦРјУИлөДОпЦККЗ_____ўЫ________Ј¬ЖдЧчУГКЗ_________ўЬ_______________:
ЈЁ3Ј©КөСйКұФЪCЦР№ЫІмөҪөГПЦПуКЗ_____________ўЭ_________________Ј¬
·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪКЗ_________________ўЮ____________________;
(4) КөСйКұФЪDЦР№ЫІмөҪөГПЦПуКЗ________________ўЯ__________________Ј¬
DЦРКХјҜөҪөДОпЦККЗ_______ўа_______,јмСйёГОпЦКөД·Ҫ·ЁәНПЦПуКЗ_________ўб_____________.
Ўҫҙр°ёЎҝ
ЎҫҪвОцЎҝ
ұҫМвҝјІй»ҜС§КөСйәНУР№Ш»ҜС§·ҪіМКҪЈ¬ЧўТв»ҜС§КөСйПЦПуөДГиКцәНКФјБөДСЎФсЎЈёщҫЭ·ҙУҰФӯАнЈ¬·ҙУҰОпОӘ°ұЖшәНСх»ҜНӯЈ¬ҝЙТФЕР¶ПКФ№ЬAОӘЦЖИЎ°ұЖшөДЧ°ЦГЈ¬ТтҙЛЧ°ИлөДТ©Ж·УҰёГОӘВИ»Ҝп§әНЗвСх»ҜёЖЈ¬°ұЖшТӘК№УГјоКҜ»ТЎЈјУИИәуЈ¬әЪЙ«Сх»ҜНӯұдОӘәмЙ«өДНӯЈ¬ЙъіЙөДЛ®әН°ұЖшЙъіЙ°ұЛ®БфФЪБЛDЦРЈ¬¶шөӘЖшНЁ№эЕЕЛ®·ЁҪшРРКХјҜЎЈјмСй°ұЖшҝЙАыУГЖдјоРФЈ¬јмСйЛ®ҝЙТФУГОЮЛ®БтЛбНӯЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘЈә2Fe2++Cl2=2Cl©Ғ+2Fe3+Ј¬2Br©Ғ+Cl2=Br2+2Cl©ҒЈ¬2Fe2++Br2=2Br©Ғ+2Fe3+ЎЈФЪbL FeBr2ИЬТәЦРНЁИлamol Cl2КұЈ¬К№ИЬТәЦР50% өДBr©ҒСх»ҜОӘBr2Ј¬ФтФӯFeBr2өДОпЦКөДБҝЕЁ¶ИОӘ
A. a/bmolL©Ғ1 B. 2a/bmolL©Ғ1 C. 3a/bmolL©Ғ1 D. 5a/bmolL©Ғ1
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјЛщКҫЈ¬AҙҰНЁИлCl2,№ШұХB·§Кұ,CҙҰКӘИуөДәмЙ«ІјМхОЮұд»ҜЈ»

ҙтҝӘB·§Кұ,CҙҰКӘИуөДәмЙ«ІјМхНКЙ«,ФтDЦРөДИЬТәКЗ ЈЁ Ј©
A. ЕЁH2SO4 B. H2O
C. NaOHИЬТә D. ұҘәНКіСОЛ®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘNaHCO3өДИЬҪв¶ИҪПРЎЎЈФЪұҘәНөДNH3әНNaClөД»мәПИЬТәЦРНЁИлCO2Ј¬ҝЙОціцNaHCO3(№ММе)ЈәNaCl+NH3+CO2+H2O=NaHCO3Ўэ+NH4ClЎЈҫЭҙЛЈ¬ОТ№ъҪЬіцөД»ҜС§јТәоөВ°сЙијЖіцБЛЙъІъҙҝјоөД·Ҫ·ЁЈә
ұҘәНNaCl(ИЬТә)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
ХвЦЦ·Ҫ·Ёұ»ИЛГЗіЖОӘәоКПЦЖјо·ЁЈ¬ҙтЖЖБЛөЫ№ъЦчТе¶ФОТ№ъҫӯјГөДТ»ЦЦ·вЛшЈ¬ҙуіӨБЛЦР№ъИЛөДГсЧеЦҫЖшЎЈ
КФ»ШҙрПВБРОКМвЈә
(1)РҙіцУЙNaHCO3№ММеЦЖИЎNa2CO3өД»ҜС§·ҪіМКҪЈә__________________ЎЈ
(2)Из№ыNa2CO3(№ММе)ЦР»мУРNaHCO3(№ММе)Ј¬УҰИзәОіэИҘ?_____________(Рҙіц·Ҫ·Ё)Ј»Из№ыNaHCO3(ИЬТә)ЦР»мУРNa2CO3(ИЬТә)Ј¬УҰИзәОіэИҘ?________(Рҙіц»ҜС§·ҪіМКҪ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТ»ЦЦРВРНМ«Сф№вөз»ҜС§өзіШЦьДЬКұөзҪвЦКИЬТәЦРАлЧУФЪБҪј«·ўЙъИзПВНјЛщКҫөДЧӘ»ҜЎЈ

ПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A. ЦьДЬКұЈ¬өзДЬЧӘұдОӘ»ҜС§ДЬәН№вДЬ
B. ЦьДЬәН·ЕөзКұЈ¬өзЧУФЪөјПЯЦРБчПтПаН¬
C. ЦьДЬКұЈ¬ЗвАлЧУУЙaј«ЗшЗЁТЖЦБbј«Зш
D. ·ЕөзКұЈ¬bј«·ўЙъЈәVO2++2H++e-=VO2++H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОТ№ъУР·бё»өДәЈЛ®ЧКФҙЈ¬ҝӘ·ўәНАыУГәЈЛ®ЧКФҙКЗөұЗ°ҝЖС§СРҫҝөДТ»ПоЦШТӘИООсЈ¬ИзНјКЗәЈЛ®ЧЫәПАыУГөДТ»ёц·ҪГжЎЈ
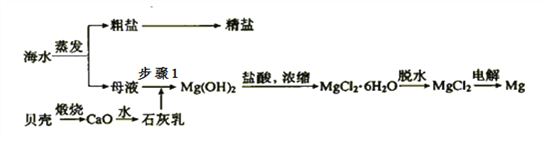
ўс.ЈЁ1Ј©ЙПКц№эіМЦРГ»УРЙжј°өҪөДЛДҙу»щұҫ·ҙУҰАаРНКЗ ______Ј»
aЈ®»ҜәП·ҙУҰ bЈ®·ЦҪв·ҙУҰ cЈ®ЦГ»»·ҙУҰ dЈ®ёҙ·ЦҪв·ҙУҰ
ЈЁ2Ј©ІҪЦи1ЦР·ЦАлІЩЧчөДГыіЖКЗ___________Ј»
ЈЁ3Ј©ҙЦСОЦРә¬УРCa2Ј«ЎўMg2Ј«ЎўSO42ЈӯөИФУЦКЈ¬ҫ«ЦЖКұЛщУГКФјБОӘЈә
a.СОЛб b.BaCl2ИЬТә c.NaOHИЬТә d.Na2CO3ИЬТә
јУИлКФјБөДЛіРтКЗ_____________Ј»
II.КөСйКТАыУГҫ«СОЕдЦЖ480mL 2.0molЎӨL1NaClИЬТәЎЈ
ЈЁ4Ј©іэИЭБҝЖҝНвЈ¬»№РиТӘөДІЈБ§ТЗЖчУР___________________Ј»
ЈЁ5Ј©УГНРЕММмЖҪіЖИЎ№ММеNaCl________gЈ»
ЈЁ6Ј©ЕдЦЖКұЈ¬°ҙТФПВјёёцІҪЦиҪшРРЈәўЩјЖЛг ўЪіЖБҝ ўЫИЬҪв ўЬАдИҙ ўЭЧӘТЖ ўЮ¶ЁИЭ ўЯТЎФИ ўаЧ°ЖҝЎЈІЩЧчЦР»№ИұЙЩТ»ёцЦШТӘІҪЦиКЗ______________________Ј»
ЈЁ7Ј©ПВБРҙнОуІЩЧчҝЙК№ЛщЕдЦЖВИ»ҜДЖИЬТәЕЁ¶ИЖ«өНөДКЗЈЁ_________Ј©
aЈ®ИЭБҝЖҝПҙҫ»әуІРБфБЛІҝ·ЦөДЛ®
bЈ®ЧӘТЖКұИЬТәҪҰөҪИЭБҝЖҝНвГж
cЈ®¶ЁИЭКұё©КУИЭБҝЖҝөДҝМ¶ИПЯ
dЈ®ТЎФИәујыТәГжПВҪөЈ¬ФЩјУЛ®ЦБҝМ¶ИПЯ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОпЦКЦРЈ¬КфУЪСОАаөДКЗЈЁЎЎЎЎЈ©
A.MgO
B.NaOH
C.H2SO4
D.BaCO3
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝCuClОӘ°ЧЙ«·ЫД©Ј¬ОўИЬУЪЛ®Ј¬ИЬУЪЕЁСОЛб»тNaClЕЁИЬТәЈ¬І»ИЬУЪТТҙјЎЈТ»ЦЦУЙәЈГаНӯ(CuәНЙЩБҝCuOөИ)ОӘФӯБПЦЖұёCuClөД№ӨТХБчіМИзПВЈә
ЈЁ1Ј©Ў°ИЬҪвҪюИЎЎұКұЈ¬ПВБРҙлК©І»ДЬМбёЯНӯөДҪюИЎВКөДКЗ__________(МоРтәЕ)ЎЈ
aЈ®Ҫ«әЈГаНӯ·ЫД©УлЛ®ҪБ°иіЙҪ¬Тә bЈ®Н¶БПКұЈ¬NaNO3ККөұ№эБҝ
cЈ®Лх¶МҪюИЎКұјд dЈ®Ҫ«ВЛФь1·ө»ШФЩҙОИЬҪвҪюИЎ
ЈЁ2Ј©Ў°»№ФӯЈ¬ВИ»ҜЎұКұЈ¬Na2SO3әНNaClөДУГБҝ¶ФCuClІъВКөДУ°ПмИзНј-1ЎўНј-2ЛщКҫЈә
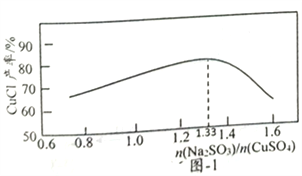

ўЩCuSO4УлNa2SO3ЎўNaClФЪИЬТәЦР·ҙУҰЙъіЙCuClөДАлБЛ·ҪіМКҪОӘ__________ЎЈ
ўЪөұn(Na2SO3)/n(CuSO4)>1.33КұЈ¬ұИЦөФҪҙуCuClІъВКФҪРЎЈ¬ЖдФӯТтКЗ__________ЎЈ
ўЫөұ1.0<n(NaCl)/n(CuSO4)<1.5КұЈ¬ұИЦөФҪҙуCuClІъВКФҪҙуЈ¬ЖдФӯТтКЗ__________ЎЈ
ЈЁ3Ј©Ў°№эВЛ2ЎұЛщөГВЛТәЦРИЬЦКөДЦчТӘіЙ·ЦОӘ__________(Мо»ҜС§КҪ)ЎЈ
ЈЁ4Ј©УГЎ°ҙјПҙЎұҝЙҝмЛЩИҘіэВЛФьұнГжөДЛ®Ј¬·АЦ№ВЛФьұ»ҝХЖшСх»ҜОӘCu2(OH)3ClЎЈCuClұ»Сх»ҜОӘCu2(OH)3ClөД»ҜС§·ҪіМКҪОӘ__________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИнГМҝуЦчТӘә¬УРMnO2(Фј70%)ЎўSiO2ЎўAl2O3Ј¬ЙБРҝҝуЦчТӘә¬УРZnS(Фј80%)ЎўFeSЎўCuSЎўSiO2ЎЈОӘБЛёЯР§АыУГХвБҪЦЦҝуКҜЈ¬ҝЖСРИЛФұҝӘ·ўБЛЧЫәПАыУГХвБҪЦЦЧКФҙөДН¬ІЫЛбҪю№ӨТХЈ¬ЦчТӘБчіМИзПВНјЛщКҫ,»ШҙрПВБРОКМв:
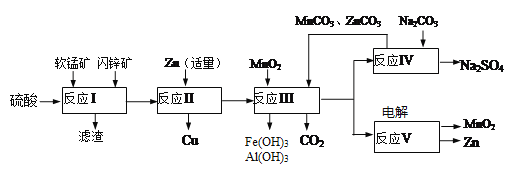
ЈЁ1Ј©·ҙУҰўсЛщөГВЛТәЦРә¬УРMn2+ЎўZn2+ЎўCu2+ЎўFe3+ЎўAl3+өИҪрКфТхАлЧУ,ЛщөГВЛТәЦРә¬УРSәН______ЎЈОӘБЛМбёЯБтЛбЎ°ЛбҪюЎұКұөДҪюіцЛЩВК,ҝЙҪшРРөДІЩЧчКЗ(ЦБЙЩБҪМх):_________ЎЈ
ЈЁ2Ј©Иф·ҙіЙўтјУИлөДРҝ№эБҝ,»№»бҪшТ»ІҪ·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪ·ҪОӘ_________ЎЈ
ЈЁ3Ј©·ҙУҰўуЦРјУИлMnO2өДЧчУГКЗЈЁАлЧУ·ҪіМКҪұнКҫ)________Ј»·ҙУҰўуЦРјУИлMnCO3ЎўZnCO3өДЧчУГКЗ________________ЎЈ
ЈЁ4Ј©·ҙУҰўхөДөзҪвЧЬ·ҙУҰОӘ:MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4Ј¬РҙіцСфј«өДөзј«·ҙУҰКҪ________________ЎЈ
MnO2+Zn+2H2SO4Ј¬РҙіцСфј«өДөзј«·ҙУҰКҪ________________ЎЈ
ЈЁ5Ј©MnO2әНZnҝЙ°ҙөИОпЦКөДБҝЦ®ұИЙъІъРҝ-ГМёЙөзіШ,ФтҙУЙъІъMnO2әНZnөДҪЗ¶ИјЖЛг,ЛщУГИнГМҝуәНЙБІщҝуөДЦКБҝұИҙуФјКЗ______ЎЈ(ұЈБфРЎКэөгәуБҪО»)
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com