
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,以下判断正确的是( )
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.BeCl2中Be采取sp2杂化 |
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:单选题
用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是
| A.CS2是V形分子 | B.SnBr2键角大于120° |
| C.BF3是三角锥形分子 | D.NH4+键角等于109.5° |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.离子晶体中可能含有共价键,一定含有金属元素 |
| B.分子晶体中可能不含共价键 |
| C.非极性分子中一定存在非极性键 |
| D.对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有机物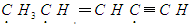 中标有“·”的碳原子的杂化方式依次为
中标有“·”的碳原子的杂化方式依次为
| A.sp、sp2、sp3 | B.sp3、sp2、sp | C.sp2、sp、sp3 | D.sp3、sp、sp2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com