

分析 实验目的是合成黄血盐,由流程可知,NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl,然后加入碳酸钠溶液可除去过量的Ca2+,经过滤后在滤液中加入KCl可转化生成K4[Fe(CN)6,说明K4[Fe(CN)6溶解度较小,以此解答该题.
(1)NaCN为强碱弱酸盐,溶液中CN-离子水解溶液呈碱性,NaCN水解呈碱性的离子方程式为:CN-+H2O?HCN+OH-,为抑制水解,在配制溶液时可将其溶解在氢氧化钠溶液中;
(2)NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl;
(3)反应器中加入氯化钙,需要加入碳酸钠除去;
(4)经过滤后在滤液中加入KCl可转化生成K4[Fe(CN)6,说明K4[Fe(CN)6溶解度较小;
(5)依据原子守恒和电子守恒配平书写化学方程式;
(6)AgCl与黄血盐制取电镀液可将其转变为K4[Ag2 (CN)6],结合电话守恒,原子守恒配书写.
解答 解:实验目的是合成黄血盐,由流程可知,NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl,然后加入碳酸钠溶液可除去过量的Ca2+,经过滤后在滤液中加入KCl可转化生成K4[Fe(CN)6,说明K4[Fe(CN)6溶解度较小,
(1)NaCN为强碱弱酸盐,溶液中CN-离子水解溶液呈碱性,NaCN水解呈碱性的离子方程式为:CN-+H2O?HCN+OH-,为抑制水解,在配制溶液时可将其溶解在氢氧化钠溶液中,在加水稀释,
故答案为:碱;NaOH;CN-+H2O?HCN+OH-;
(2)NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl,离子方程式为:K++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]↓,
故答案为:K++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]↓;
(3)反应器中加入氯化钙,加入碳酸钠溶液可除去过量的Ca2+,
故答案为:除去其中的Ca2+;
(4)经过滤后在滤液中加入KCl可转化生成K4[Fe(CN)6,说明K4[Fe(CN)6溶解度较小,故答案为:>;
(5)依据K4Fe(CN)6的系数为3,结合原子守恒,Fe3C前系数为3,KCN前系数为12,电子守恒得到N2前系数为1,依据氮原子守恒,(CN)2前系数为2,碳原子守恒,C前系数为1,配平得到的化学方程式为:3K4Fe(CN)6=Fe3C+12KCN+N2↑+C+2(CN)2↑,
故答案为:12,1,1,2,1;
(6)电镀液不能直接用硝酸银溶液,可将其转变为K4[Ag2 (CN)6],AgCl与黄血盐制取电镀液可将其转变为K4[Ag2 (CN)6],反应的离子方程式为:2AgCl+[Fe(CN)6]4-=Fe2++[Ag2 (CN)6]4-+2Cl-,
故答案为:2AgCl+[Fe(CN)6]4-=Fe2++[Ag2 (CN)6]4-+2Cl-.
点评 本题考查物质的制备实验方案的设计,侧重于学生的分析能力、实验能力和计算能力的考查,为高考常见题型,注意根据流程图把握实验的原理和操作方法,难度中等,注意根据氧化还原反应的化合价的升降总数相等计算.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 3:2:1 | B. | 2:6:3 | C. | 3:6:2 | D. | 2:1:3 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考一化学试卷(解析版) 题型:实验题
某学生通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
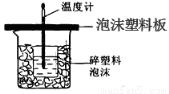
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________;由图可知该装置有不妥之处? 。
(2)实验中改用60 mL0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相 等”);所求中和热的数值会______________(填“相等”或 “不相等”)。
等”);所求中和热的数值会______________(填“相等”或 “不相等”)。
(3)该同学做实验时有些操作不规范,造成测得中和热的数 值偏低,请你分析可能的原因
值偏低,请你分析可能的原因 是
是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视计数
E.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
(4)将V1ml 1.0mol/L HCl溶液和V2ml未知浓度的NaOH溶液混合均匀后测量并记录温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)

通过分析图像可知,做该实验时环境温度 (填“高于”,“低于”或“等于”)22℃,该NaOH溶液的浓度约为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上月考一化学卷(解析版) 题型:计算题
磷在氧气中燃烧,可能生成两种固态氧化物。6.2 g的单质磷(P)在6.4 g氧气中燃烧,至反应物耗尽,并放出a kJ热量。
(1 )通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
)通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
(2)已知单质磷的燃烧热为b kJ/mol,则1mol P与O2反应生成固态P2O3的反应热ΔH= 。
(3)写出1mol P与O2反应生成固态P2O3的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上月考一化学卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)===2H2O(l);ΔH=-571.6 kJ·mol-1
CO(g)+ O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1
O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1
现有CO、H2和CO2组成的混合气体112.0 L(标准状况)完全燃烧后放出的总热量为851.4 kJ,并生成18 g液态水。则燃烧前混合气体中CO的体积分数为
A.80% B.40% C.60% D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
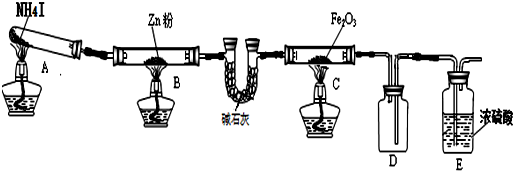
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无明显变化 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅含有碳和氢两种元素的化合物称为烃 | |
| B. | 凡是分子里含碳元素的化合物都属于烃 | |
| C. | 甲烷可以使酸性高锰酸钾溶液褪色 | |
| D. | 有机化合物分子中碳原子之间只有单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | WZ2分子中所有原子最外层都为8电子结构 | |
| B. | WX2、ZX2的化学键类型相同 | |
| C. | 原子半径大小顺序为X<W<Y<Z | |
| D. | 非金属性Y<Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com