
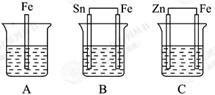
 (填 “变大”“变小”或“不变”)。
(填 “变大”“变小”或“不变”)。

科目:高中化学 来源:不详 题型:单选题
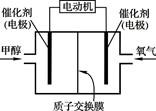
| A.外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B.通甲醇一端为负极 |
| C.正极反应为:O2+4H++4e-= 2H2O |
| D.负极反应为:CH3OH+H2O+6e-= CO2↑+6H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
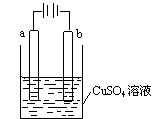
| A.若a和b为石墨,通电后a电极上发生的反应为Cu2++2e-=Cu |
| B.若a和b为铜,通电后a电极有气体产生 |
| C.若a为铜,b为铁,通电后Cu2+向a电极移动 |
| D.若a为粗铜,b为纯铜,通电后b电极质量增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.手机上用的锂离子电池属于二次电池 |
| B.铅蓄电池中负极为铅,电解质是硫酸 |
| C.氢氧燃料电池正极输入氢气,负极输入空气 |
| D.锌锰干电池即使不用,长久放置也会失效 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 序号 | A | B | C | D | E |
| 污水类型 | 生活污水 | 印染 | 电镀 | 造纸 | 硫酸工业废水 |
| COD值/mg·L-1 | 520 | 870 | 20 | 960 | 120 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com