
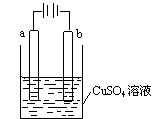
| A.若a和b为石墨,通电后a电极上发生的反应为Cu2++2e-=Cu |
| B.若a和b为铜,通电后a电极有气体产生 |
| C.若a为铜,b为铁,通电后Cu2+向a电极移动 |
| D.若a为粗铜,b为纯铜,通电后b电极质量增加 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
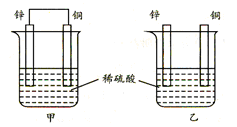
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,电极反应:2H++2e→H2↑;乙中锌片是负极, 电极反应:Zn-2e→Zn2+ |
| C.两烧杯中的pH值均增大 |
| D.产生的气泡速率甲比乙慢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
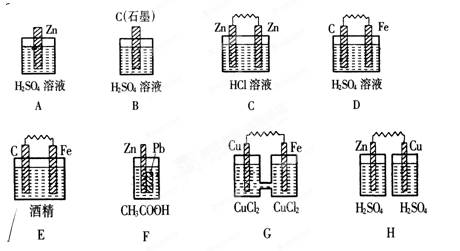
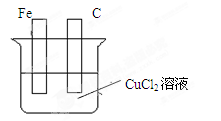
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
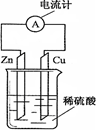
| A.电子由铜片通过导线流向锌片 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.锌片逐渐溶解 |
| D.该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
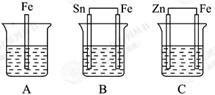
 (填 “变大”“变小”或“不变”)。
(填 “变大”“变小”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
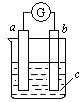
| A.a是锌,b是铜,c是稀硫酸溶液 |
| B.a是铁,b是银,c是硝酸银溶液 |
| C.a是银,b是铁,c是硝酸银溶液 |
| D.a是碳,b是铁,c是氯化铜溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.电池反应中有NaCl生成 |
| B.电池的总反应是金属钠还原三价铝离子 |
| C.正极反应为:NiCl2+2e-=Ni+2Cl- |
| D.钠离子通过钠离子导体在两电极间移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.金属活动性铝比镁强 |
| B.金属活动性镁比铝强,两装置中镁均为负极 |
| C.仅根据金属活动性顺序不能准确判断原电池的正负极 |
| D.原电池中的正负极受电解质溶液的酸碱性、强氧化性等因素的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com