
| A.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在 |
| B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在 |
| C.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在 |
| D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在 |
科目:高中化学 来源:不详 题型:单选题
| A.无色溶液中:K+、H+、Fe2+、NO3- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.含0.1mol·L-1 HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42- |
| D.含0.1 mol·L-1 SCN-的溶液中:Fe3+、NH4+、NO3-、Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
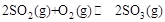 。
。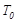 ℃时,将2mol
℃时,将2mol 和1.5 mol
和1.5 mol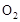 充入2L密闭容器中发生上述反应,容器中
充入2L密闭容器中发生上述反应,容器中 的物质的量随温度变化的曲线如图所示。
的物质的量随温度变化的曲线如图所示。
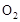 ,同时生成2mol
,同时生成2mol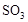
 、
、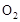 、
、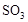 的浓度之比为2∶1∶2
的浓度之比为2∶1∶2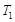 ℃时,上述反应的化学平衡常数K= 。
℃时,上述反应的化学平衡常数K= 。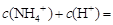 。
。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
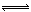 2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别是0.1mol·L-1、0.4mol·L-1、0.2mol·L-1、0.3mol·L-1当反应达到平衡后,各物质的物质的量浓度不可能是
2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别是0.1mol·L-1、0.4mol·L-1、0.2mol·L-1、0.3mol·L-1当反应达到平衡后,各物质的物质的量浓度不可能是 | A.c(X2)="0.15" mol·L-1 | B.c(Y2)="0.9" mol·L-1 |
| C.c(Z2)="0.3" mol·L-1 | D.c(Q2)="0.5" mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H+、Na+、CO32-、Cl- | B.Ag+、Al3+、NO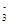 、H+ 、H+ |
| C.K+、H+、SO42-、OH- | D.Ba2+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
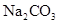 、
、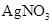 、
、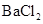 、
、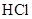 四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙
四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙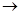 沉淀;甲+丙
沉淀;甲+丙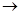 沉淀;乙+丙
沉淀;乙+丙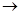 沉淀;丙+丁
沉淀;丙+丁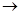 沉淀;乙+丁
沉淀;乙+丁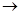 无色无味气体。则甲、乙、丙、丁四种溶液依次是( )
无色无味气体。则甲、乙、丙、丁四种溶液依次是( )A.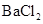 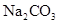 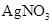 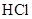 | B.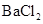 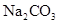 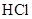 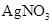 |
C.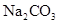 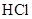 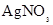 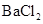 | D.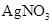 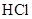 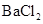 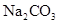 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
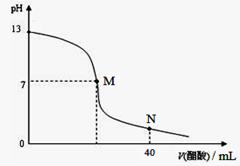
| A.在M点,两者恰好反应完全 |
| B.滴定前,酸中c(H+) 等于碱中c(OH-) |
| C.NaOH溶液的物质的量浓度为0.1 mol/L |
| D.在N点,c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
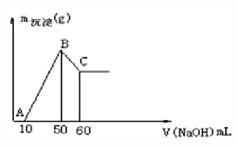
| A.1:1:1 | B.2:2:1 | C.2:1:1 | D.1:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com