
 �ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ�����֮���������ת����ϵ��
�ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ�����֮���������ת����ϵ��
| ||
| ||
| ||
| ||
| 3.36g |
| 56g/mol |
| 1.12L |
| 22.4L/mol |
| 3.36g |
| 56g/mol |
| 1.12L |
| 22.4L/mol |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2011?������ģ�⣩�ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ���Ӧ���£���+�ҡ���+��
��2011?������ģ�⣩�ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ���Ӧ���£���+�ҡ���+��| 2 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2010?������һģ���ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ�����֮���������ת����ϵ����+�ҡ���+��
��2010?������һģ���ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ�����֮���������ת����ϵ����+�ҡ���+��

| ||
| ||
| 2 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ס��ҡ����������ɶ�����Ԫ����ɵ��������ʣ�����֮���������ת����ϵ����+�ҡ���+��
�ס��ҡ����������ɶ�����Ԫ����ɵ��������ʣ�����֮���������ת����ϵ����+�ҡ���+��| 2 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ס��ҡ����������ɶ�����Ԫ����ɵ����ʣ�����֮���������ת����ϵ����+��![]() ��+��
��+��
��1��ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ������Ϊˮ��
�� ����Ϊ��״���壬��Ϊ��ȼ�����壬������ڼȺ��м��Լ��ֺ��зǼ��Լ�������ĵ���ʽ�� ��
����������N��ClԪ����ɵĻ��������ӽṹģ������ͼ��ʾ��������Ư���ԡ������ClԪ�صĻ��ϼ��� ��
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊˮ��
�� ���ͱ���ͬ����Ԫ����ɵĵ��ʣ�����ɼ�Ԫ��λ�ڵ������ڣ��˷�Ӧ�����ӷ���ʽ�� ��
�� �����Ͷ�������һ�������»�ԭ![]() ���˷�Ӧ�Ļ�ѧ����ʽ�� ��
���˷�Ӧ�Ļ�ѧ����ʽ�� ��
�� ��������N��OԪ����ɵ���̬���ʣ��ʺ���ɫ����3.36 g![]() �ӵ�һ��������Һ�У��ռ���1.12 L���嶡��������Ϊ��״��������Ӧ�����ӷ���ʽ�� ��
�ӵ�һ��������Һ�У��ռ���1.12 L���嶡��������Ϊ��״��������Ӧ�����ӷ���ʽ�� ��
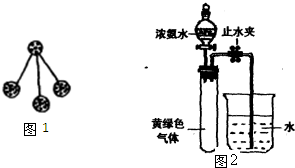
��3��Hofmann��������ת����ϵ�ⶨ�����ӵ���ɡ���������ͼ��ʾ��װ�ý���ʵ�飬��Һ©���Ļ���������Ũ��ˮ�������ٷ�ӦΪֹ���رշ�Һ©���Ļ��������ָ������£���ֹˮ�У��Թ���Һ��������![]() ����
����
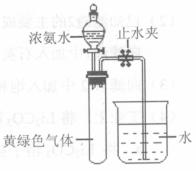
�� ����Ũ��ˮһ��ʱ����Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ�� ��
�� ֤���Թ��ڡ����ٷ�Ӧ����ʵ������������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com