
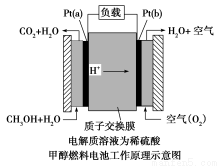
近几年开发的甲醇燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:
请回答下列问题:
(1)Pt(a)电极是电池的 极,电极反应式为 ;Pt(b)电极发生 反应(填“氧化”或“还原”),电极反应式为 。
(2)电池的总反应方程式为 。
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有 mol。
(1)负 2CH3OH+2H2O-12e-=2CO2↑+12H+ 3O2+12H++12e-=6H2O
(2)2CH3OH+3O2=2CO2+4H2O
(3)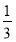
【解析】从示意图中可以看出电极Pt(a)原料是CH3OH和水,反应后产物为CO2和H+,CH3OH中碳元素化合价为-2,CO2中碳元素化合价为+4,说明Pt(a)电极上CH3OH失去电子,电极Pt(a)是负极,则电极Pt(b)是正极,Pt(b)电极原料是O2和H+,反应后的产物为H2O,氧元素化合价由0→-2,发生还原反应,因为电解质溶液是稀H2SO4,可以写出电池总反应式为2CH3OH+3O2=2CO2+4H2O,再写出较为简单的正极反应式:3O2+12e-+12H+=6H2O,用总反应式减去正极反应式即可得到负极反应式为:2CH3OH+2H2O-12e-=2CO2↑+12H+。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014年高考化学二轮复习专题滚动练1 化学基本概念练习卷(解析版) 题型:选择题
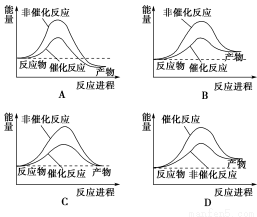
据报道,科学家研制出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是( )
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后训练专题练习卷一(解析版) 题型:填空题
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是
Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)。
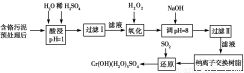
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 11.1 | 8 | 9(>9溶液) |
部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见上表。
(1)酸浸时,为了提高浸取率可采取的措施为________________(至少写一条)。
(2)调pH=8是为了除去________(填Fe3+、Al3+、Ca2+、Mg2+,下同)。
(3)钠离子交换树脂的原理为Mn++nNaR―→MRn+nNa+,被交换的杂质离子是________。
(4)试配平反应方程式:
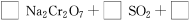
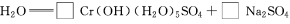 ;
;
生成1 mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练9-2练习卷(解析版) 题型:填空题
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法之一是电解法。
(1)该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。用Fe作电极的原因为 。
(2)在阴极附近溶液pH升高的原因是(用电极反应解释) ,溶液中同时生成的沉淀还有 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练9-2练习卷(解析版) 题型:选择题
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
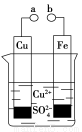
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为Cu2++2e-=Cu
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练9-1练习卷(解析版) 题型:选择题
一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO2-+H2O。下列说法不正确的是( )
A.该电池的优点是电极材料和电解质用完后可以更换
B.该电池发生氧化反应的是金属铝
C.电极的正极反应式为3ClO-+3H2O+6e-=3Cl-+6OH-
D.当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练9-1练习卷(解析版) 题型:选择题
将两金属A、B分别用导线相连接,并同时插入电解质溶液中,发现A极的质量增加,则下列说法正确的是( )
A.金属活动性:A>B
B.A极是正极,电解质溶液可以是盐酸
C.B极是负极
D.要判断A极与B极是正极还是负极,还需考虑电解质溶液
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练8-3练习卷(解析版) 题型:填空题
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
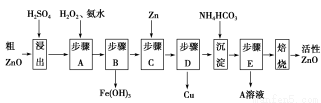
已知:几种离子生成氢氧化物沉淀时的pH如表:
待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是 ,该步骤需控制溶液pH的范围是 。
(2)A溶液中主要含有的溶质是 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为 mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-3练习卷(解析版) 题型:填空题
甲醇可通过将煤气化过程中生成的CO和H2在一定条件下,发生如下反应制得:CO(g)+2H2(g)  CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
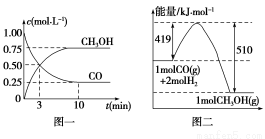
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)= ,CO的转化率为 。
(2)该反应的平衡常数表达式为 ,温度升高,平衡常数 (填“增大”、“减小”或“不变”)。
(3)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则加入各物质后该反应向 (填“正”、“逆”)反应方向移动,理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com