
����ʯ����ѧʽ��ʾΪMgCO3��CaCO3��Ϊԭ���Ʊ�������þ�Ĺ����������£�

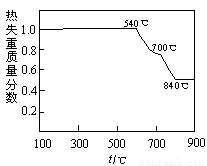
��1����������ͼ�жϰ���ʯ�����ա������������Ҫ�ɷ� _____ �������ա��¶�Ӧ������ _____ ��
��2������ͼ�С����ȷ�Ӧ���Ļ�ѧ����ʽΪ _ _________________________ ��
��3������������Һ��pH=9.5����ʱ��Һ��c(Mg2+)= _______ ����֪Ksp[Mg(OH)2]=5.61��10-12����
��4���ù����п���ѭ��ʹ�õ������� �� ���ѧʽ����
��5����ͳ���ս�����ʯ�ֽ�Ϊ����þ�������ƺ���ȡ���ù��ղ������հ���ʯ �ķ��������ŵ��� �� ��
��1��CaCO3��MgO��2�֣���700�� ��2�֣�
��2��(NH4)2SO4+MgO  MgSO4+2NH3��+H2O
��2�֣�
MgSO4+2NH3��+H2O
��2�֣�
��3��5.61��10-3mol��L-1��2�֣�
��4����(NH4)2SO4 ��2�֣���NH3��NH3��H2O
��5��������Դ���ģ�2�֣�������CaCO3���루2�֣�(����������Ҳ���֣��磺����CO2�ŷ�)
��������
�����������1���ӹ����п��Եõ�CaCO3���������жϣ���֪�ֽ��ֻ��̼��þ���ӱ��п��Կ������¶ȵ���540�� ʱ�����ʲ��ֽ⣬����840��
ʱ��̼��ƺ�̼��þ���ֽ⣬��˸��¶Ȳ�����700�档��2�����ȵĹ����Ƿų������Ĺ��̣��ù�������Ϊ����þ��ˮ��Ӧ���٣�����漰���ķ�ӦӦ��Ϊ��(NH4)2SO4+MgO
 MgSO4+2NH3��+H2O
MgSO4+2NH3��+H2O
��3��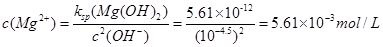
��4��(NH4)2SO4 ��2�֣���NH3��NH3��H2O
��5��������Դ���ġ�����CaCO3���롣
���㣺�������ʵ��Ʊ���


 Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Ȼ�������һ�ְ���ʯ�Ŀ�ʯ���仯ѧʽ��xCaCO3?yMgCO3������Ϊԭ�ϣ�����ȡ�ͻ���ϵȣ�
��Ȼ�������һ�ְ���ʯ�Ŀ�ʯ���仯ѧʽ��xCaCO3?yMgCO3������Ϊԭ�ϣ�����ȡ�ͻ���ϵȣ�| ���� |
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡտ������ͨ�߿����ԣ��������ۻ�ѧ�Ծ��������棩 ���ͣ������
����ʯ����ѧʽ��ʾΪMgCO3��CaCO3��Ϊԭ���Ʊ�Mg(OH)2�Ĺ�����������ͼ��ʾ��

��1����ĥ�������� ��
��2���ù����п�ѭ��ʹ�õ������� �� ��д��ѧʽ����
��3������ʯ���յ���Ҫ������MgO��CaCO3������ͳ�����ǽ�����ʯ���ȷֽ�ΪMgO��CaO����ȡ������ʯ���յ��ŵ��� ��
��4�����ȷ�Ӧ�����ӷ���ʽΪ ��
��5���ټ��ȷ�Ӧʱ����323k��353k��Һ��c(NH4+)�뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ��������ͼ����373k�����ߡ�

����ͼ��֪�������¶����ߣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʯ����ѧʽ��ʾΪMgCO3��CaCO3��Ϊԭ���Ʊ�Mg(OH)2�Ĺ�����������ͼ��ʾ��
��1����ĥ������������ _�� ���������õIJ����������ձ��� _�� �� _�� ��
��2���ù����п�ѭ��ʹ�õ����������� _�� ���� _�� ��д��ѧʽ����
��3������ʯ���յ���Ҫ������MgO��CaCO3������ͳ�����ǽ�����ʯ���ȷֽ�ΪMgO��CaO����ȡ������ʯ���յ��ŵ������� _������ ��
��4�����ȷ�Ӧ�����ӷ���ʽΪ���������� _�������� ��
 ��5���ټ��ȷ�Ӧʱ����323k��353k��Һ��c(NH4+)�뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ��������ͼ����373k�����ߡ�
��5���ټ��ȷ�Ӧʱ����323k��353k��Һ��c(NH4+)�뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ��������ͼ����373k�����ߡ�
����ͼ��֪�������¶����ߣ����������� _���������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com