
【题目】Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:

(1)A、B、C三者的关系是___。
(2)A的分子式为___,C的名称为__。
(3)写出C的同分异构体的结构简式:___。
Ⅱ.如图均能表示甲烷的分子结构,其中更能反映其真实的存在状况的是__(填字母)。


【答案】同系物 C2H6 正丁烷 (CH3)2CHCH3 D
【解析】
烷烃由C和H元素组成,大球表示C,小球表示H,其通式为CnH2n+2,所以A、B、C的结构简式为CH3CH3、CH3CH2CH3、CH3CH2CH2CH3。
(1)三者的关系为碳原子数不同的烷烃,应属同系物,故答案为:同系物;
(2)根据图示可知,A的分子式为:C2H6,C的名称为正丁烷,故答案为:C2H6,正丁烷;
(3)丁烷的同分异构体为异丁烷,其结构简式为:(CH3)2CHCH3,故答案为:(CH3)2CHCH3;
Ⅱ.由于比例模型表示的是原子的相对大小及连接形式,更接近分子的真实结构,所以D正确,故答案为:D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸厂的酸性废水中砷(As)元素(主要以 H3AsO3 形式存在)含量极高,为控制砷的排放, 某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多 2 个电子层,砷在元素周期表的位置为_____。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反 应的离子方程式为_____。
(2)电镀厂的废水中含有的 CN-有剧毒,需要处理加以排放。处理含 CN-废水的方法之一是在 微生物的作用下,CN-被氧气氧化成 HCO3- ,同时生成 NH3,该反应的离子方程式为_____。
(3)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子, A―表示乳酸根离子):
①阳极的电极反应式为_____
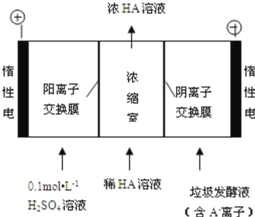
②电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的 OH-可忽略不 计。400 mL 10 g·L-1 乳酸溶液通电一段时间后, 浓度上升为 145 g/L(溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为_____L (已知:乳酸的摩尔质量为 90 g/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是
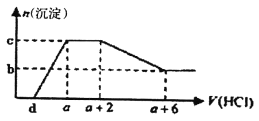
A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积相同的恒容密闭容器中发生反应:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
C(s) | H2O(g) | CO(g) | H2(g) | CO(g) | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0 | 0.4 |
Ⅱ | 500 | 0 | 0 | 2.0 | 2.0 | |
Ⅲ | 400 | 1.0 | 1.0 | 0 | 0 | 0.3 |
下列说法正确的是
A.该反应的正反应为吸热反应
B.达到平衡时,容器内的压强:2PⅠ<PⅡ
C.达到平衡时,反应物的转化率αⅠ(H2O)+αⅡ(CO)<1
D.若起始时向容器Ⅰ中加入2.7 mol C(s)、0.4mol H2O(g)、0.6mol CO(g)和0.6mol H2(g),则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是( )
A. 右图表示反应①中的能量变化

B. 可推知2H2(g)+O2(g)=2H2O(g) ΔH=-483.8 kJ/mol
C. 1 mol CH3OH充分燃烧放出的热量为192.9 kJ
D. CH3OH转变成H2的过程一定要吸收能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiO2广泛应用于涂料、塑料、造纸、印刷油墨等领域。TiOSO4溶液加水稀释可析出aTiO2·bH2O沉淀。
(1)写出TiOSO4溶液加水稀释时所发生反应的化学方程式:____。
(2)实验室测定aTiO2·bH2O组成的方法如下:
步骤一:取样品4.900 g,在酸性条件下充分溶解,加入适量铝将溶解生成的TiO2+还原为Ti3+,将溶液转移到容量瓶中,并定容至250 mL。
步骤二:取25.00 mL定容后的溶液于锥形瓶中,加入KSCN溶液作指示剂,用0.2000mol·L-1的NH4Fe(SO4)2 标准溶液滴定,将实验数据记录在下表中。重复滴定2次。滴定过程发生的物质转化为:Ti3+![]() TiO2+
TiO2+
滴定序号 | 待测液体积/mL | NH4Fe(SO4)2标准溶液 | |
滴定管起点读数/mL | 滴定管终点读数/mL | ||
1 | 25.00 | 0.04 | 25.04 |
2 | 25.00 | 0.07 | 25.05 |
3 | 25.00 | 0.13 | 25.15 |
①使用滴定管过程中所涉及下列操作的先后顺序是____(填字母)。
a.排除滴定管尖嘴处的气泡 b.检查滴定管是否漏液 c.用待装液润洗滴定管
②滴定终点的实验现象是____。
③通过计算确定该样品的组成,写出计算过程____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示与对应的叙述符合的是( )
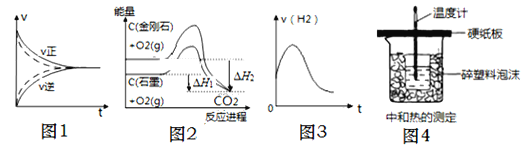
A.图1,实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化
B.图2,反应C(金刚石,s)=C(石墨,s)的焓变ΔH=ΔH1-ΔH2
C.图3,表示除去氧化膜的镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因可能是该反应为放热反应
D.用图4所示装置可以测中和热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向1molL﹣1的Na2CO3溶液中加酚酞试液,观察到的现象是_____,原因是(离子方程式表示)_____。再向溶液中滴入过量的氯化钙溶液,观察到的现象_____,原因是(用离子方程式表示和必要的语言说明)_____
(2)某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂用盐酸滴定待测液NaOH,判断滴定终点时的方法是______;若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度值_____(填“无影响”、“偏高”或“偏低”)
(3)某温度下,纯水的c(H+)=3×10﹣7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH﹣)的比值为______。
(4)加热蒸干并灼烧AlCl3溶液的产物是______;加热蒸干并灼烧FeCl2溶液的产物是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________;若有1mol硝酸铵完全分解,则转移电子的数目为___________(设NA为阿伏加德罗常数的值)。
(2)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-![]() O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
①该反应在60~90s与90~120s内的平均反应速率分别约为___________,___________;比较两者大小可得出的结论是______________________。
②计算T℃时该反应的平衡常数为______________________。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________(写出一条即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com