
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是( )
A. 右图表示反应①中的能量变化

B. 可推知2H2(g)+O2(g)=2H2O(g) ΔH=-483.8 kJ/mol
C. 1 mol CH3OH充分燃烧放出的热量为192.9 kJ
D. CH3OH转变成H2的过程一定要吸收能量
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学为家乡农业生产提出了下列建议,其中不合理的是( )
A.要加大灌溉用水的管理力度,防止水资源的污染和浪费
B.禁止就地焚烧农作物秸秆,应该将其回收用于制沼气
C.用熟石灰改良酸性土壤,应同时施加碳铵(NH4HCO3)以提高土壤肥力
D.要综合利用农家肥和化肥,重视在增施农家肥的基础上,配合使用化肥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和钙的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)钙元素的焰色反应呈砖红色,其中红色对应的辐射波长为_____(填字母)nm。
A.435 B500 C.580 D.605 E. 700
(2)元素S和Ca中,第一电离能较大的是_____(填元素符号),其基态原子核外电子排布式为_______。
(3)X射线衍射测定等发现,石膏(CaSO4 2H2O)中存在SO42-离子。SO42-离子的几何构型为_____,中心原子的杂化形式为________。
(4) 基态Ca原子中,核外电子占据最高能层的符号是____,占据该能层电子的电子云轮廓图形状为_____。钙元素和锰元素属于同一周期,且核外最外层电子构型相同,但金属钙的熔点、沸点等都比金展锰低,原因是_________________。
(5)过氧化钙晶体的晶胞结构如图所示,已知该晶胞的密度是ρ g cm-3,则晶胞结构中最近的两个Ca2+间的距离为______ (列算式即可,用NA表示阿伏加德罗常数的数值)nm,与Ca2+紧邻O22-的个数为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂试剂选择正确的是
选项 | 待提纯物质 | 杂质 | 除杂试剂 |
A | Cl2 | HCl | NaOH溶液 |
B | CO2 | CO | O2 |
C | FeCl3溶液 | FeCl2 | Cl2 |
D | Na2CO3 | NaHCO3 | 盐酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1反应过程的能量变化如图所示.请回答下列问题: 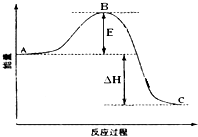
(1)图中A、C分别表示、 , E的大小对该反应的反应热有无影响? . 该反应通常用催化剂,加催化剂后会使图中B点升高还是降低? , 理由是;
(2)已知单质硫的燃烧热为296KJmol﹣1 , 写出由S(s)生成SO3(g)的热化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,由水电离生成的c(H+)为1.0×10-12mol·L-1下列说法正确的是( )
A. 一定是酸溶液 B. 一定是碱溶液
C. 一定是显碱性的溶液 D. 可能是酸溶液,也可能是碱溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去括号内杂质的方法正确的是( )
A.FeCl2(FeCl3):加入足量铁屑,充分反应后过滤
B.CO2(HCl):通过饱和NaOH溶液,收集气体
C.N2(O2):通过灼热的CuO粉末,收集气体
D.KCl (MgCl2):加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBH4( 硼氢化钠)广泛用于贮氢、有机合成及纳米材料制取等。回答下列问题:
(1)NaBH4的电子式为_________。
(2) NaBH4水解生成H2同时生成NaBO2,每生成1mol H2 转移电子数为______个;Kreevoy 等提出在碱性溶液中该水解反应的半衰期t1/2(反应物浓度减少一半所需时间) 与温度的关系式为l gt1/2=pH-(0.034T-1.92),其他条件相同时,贮氢时为减慢水解速率,应控制pH 及T的条件是______;已知0℃、pH=10时半衰期为4.32×102min,若此时NaBH4的依度为4.32 molL.1,则t0至半衰期生成H2的平均速率为_________molL-1min-1。
(3)直接NaBH4碱性燃料电池的结构如下图所示:
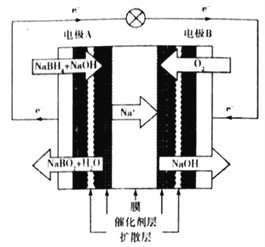
电池工作时,电极B周围溶液的pH______ (填“升高”“降低”或“不变”),电极A 上发生的电极反应式为_________________。
(4)制取NaBH4的方法之一是将Na2B4O7、SiO2 及金属Na按一定比例混合通H2 并加热到360- 370 ℃(同时生成Na2SiO3),该反应的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com