
【题目】已知A、B、C、D为短周期内原子半径依次增大的元素,X、 Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、 乙为其中两种元素对应的单质。若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如下图所示(部分反应物或生成物省略),则下列说法中不正确的是

A. 相对分子质量M>N,沸点N>M
B. 简单离子半径:C2—>B2—>D+>A+
C. A、C、D的常见氧化物相互之间一定能反应
D. D与其他元素均能形成离子化合物
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述,正确的是( )
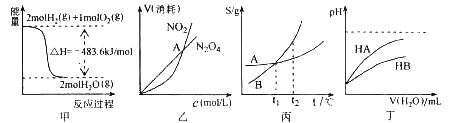
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJmol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数A=B
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定的
①气体分子的直径②气体物质的量的多少 ③气体分子间的平均距离 ④气体分子的相对分子质量
A. ①② B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.15mol的MnO2与过量的12mol/L的浓盐酸反应,与50ml 12mol/L的浓盐酸与过量MnO2反应,两者产生的氯气相比(其它反应条件相同)
A.一样多 B.前者较后者多 C.后者较前者多 D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 浊液的分散质粒子直径大于l00nm,不能通过滤纸
B. 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸
C. 利用丁达尔效应可以区分溶液和胶体
D. 将氯化铁浓溶液和氢氧化钠浓溶液混合,能得到氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把5.1 g铝镁合金的粉末放入100 mL某盐酸中,恰好完全反应得到5.6 L H2(标准
状况下)。试计算:
(1) 上述反应过程中,转移电子的物质的量;
(2) 该盐酸的物质的量浓度;
(3) 该合金中铝的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com