
| A�� | �٢� | B�� | �٢� | C�� | �٢ڢ� | D�� | �� |
���� ��Ԫ�ػ��ϼ۱仯�ķ�Ӧ��Ϊ������ԭ��Ӧ������Ԫ�ػ��ϼ۱仯�ķ�Ӧ��Ϊ��������ԭ��Ӧ���Դ������
��� �⣺��2Fe+O2+2H2O=2Fe��OH��2��Fe��OԪ�صĻ��ϼ۱仯��Ϊ������ԭ��Ӧ��
��4Fe��OH��2+O2+2H2O=4Fe��OH��3��Fe��OԪ�صĻ��ϼ۱仯��Ϊ������ԭ��Ӧ��
��2Fe��OH��3=Fe2O3+3H2O������Ԫ�ػ��ϼ۱仯�ķ�Ӧ��Ϊ��������ԭ��Ӧ��
�������ڷ�������ԭ��Ӧ���Ǣۣ�
��ѡD��
���� ���⿼��������ԭ��Ӧ�����շ����ķ�Ӧ����Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ��Ͷ��һС������� | B�� | ��ˮ��ͨ����������� | ||
| C�� | ��ˮ������� | D�� | ��ˮ�м������ƾ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ΪAl��OH��3 | B�� | ǰ��ΪAl2O3������ΪNaAlO2 | ||
| C�� | ��ΪAl2O3 | D�� | ǰ��ΪAlCl3������ΪNaAlO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۻ�������һ���������Ӽ� | |
| B�� | ���ӻ�������һ���������ۼ� | |
| C�� | ����Խ���ý�����Խǿ | |
| D�� | ˫ԭ�ӷ����й��ۼ�Խǿ���е�Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
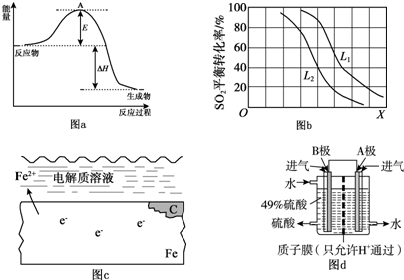
 H2SO32H2SO3+O2
H2SO32H2SO3+O2 2H2SO4��
2H2SO4�� 2SO3��Ӧ�ġ�H=-198kJ/mol���Ƿ��ȷ�Ӧ����ѹǿһ��ʱ���¶����ߣ�ƽ�����ƣ�SO2ƽ��ת���ʼ�С��
2SO3��Ӧ�ġ�H=-198kJ/mol���Ƿ��ȷ�Ӧ����ѹǿһ��ʱ���¶����ߣ�ƽ�����ƣ�SO2ƽ��ת���ʼ�С���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
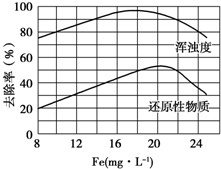 FeCl3���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3��Ч���Ҹ�ʴ��С����ش��������⣺
FeCl3���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3��Ч���Ҹ�ʴ��С����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
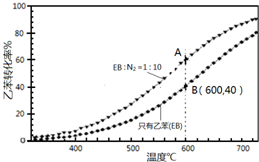 ����ϩ��
����ϩ�� ���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã�
���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã� CH2CH3��g��$\stackrel{����}{?}$
CH2CH3��g��$\stackrel{����}{?}$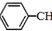 =CH2��g��+H2��g����=+QkJ��mol-1
=CH2��g��+H2��g����=+QkJ��mol-1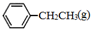 ��
��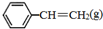 ��H2��g����ȼ���ȣ���H���ֱ�Ϊ-Q1 kJ•mol-1��-Q2kJ•mol-1��-Q3 kJ•mol-1��д��Q��Q1��Q2��Q3�Ĺ�ϵʽQ2+Q3-Q1��
��H2��g����ȼ���ȣ���H���ֱ�Ϊ-Q1 kJ•mol-1��-Q2kJ•mol-1��-Q3 kJ•mol-1��д��Q��Q1��Q2��Q3�Ĺ�ϵʽQ2+Q3-Q1���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com