
【题目】钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
①TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
②TiCl4+2Mg![]() 2MgCl2+Ti
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A. 反应①中碳元素被还原 B. 反应②中钛元素被氧化
C. 反应①中Cl2是还原剂 D. 反应②中TiCl4是氧化剂
科目:高中化学 来源: 题型:
【题目】如图所示的装置,打开分液漏斗的活塞,让水滴入锥形瓶中可以看到水浮在硫酸上面且水立即沸腾,硫酸液滴飞溅,同时U形管中甲端下降,乙端上升.这个实验说明了、 , 这个事实告诉我们为了防止发生事故,在稀释浓硫酸时,一定要 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关浓硫酸的性质或作用,叙述错误的是
A.浓硫酸的脱水性是化学性质
B.使铁、铝钝化表现了强氧化性
C.制备乙酸乙酯的反应中起催化吸水作用
D.与氯化钠固体共热制氯化氢气体时,表现强酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 阴离子只有还原性
B. 含有最高价元素的化合物,只有氧化性,不具有还原性
C. Zn和稀硫酸反应既属于离子反应,也属于氧化还原反应
D. 没有单质参加也没有单质生成的反应一定不是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
A. 若产物为NaClO、NaCl,则吸收后的溶液中n(ClO-)=n(Cl-)
B. 若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
C. 若产物为NaClO、NaClO3、NaCl,则由吸收后的溶液中n(Cl-)和n(ClO-)可计算吸收的n(Cl2)
D. 若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列符合实际并用于工业生产的是
A.工业炼铝:电解熔融的氯化铝
B.制取漂粉精:将氯气通入澄清石灰水
C.工业制硫酸:用硫磺为原料,经燃烧、催化氧化、最后用98.3%浓硫酸吸收
D.工业制烧碱:电解饱和食盐水,在阳极区域得到烧碱溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金在工业上有着广泛的用途,氧化铝是冶炼金属铝的主要原料。从铝土矿(主要成分是Al2O3,含有SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
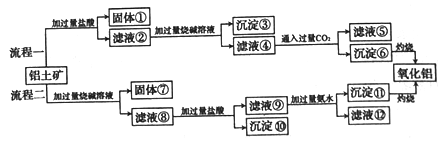
回答下列问题:
(1)Al2O3、SiO2、Fe2O3、MgO四种物质中,属于酸性氧化物的是______,属于碱性氧化物的是______。
(2)流程一中,沉淀③是_________(填化学式,下同),沉淀⑥是_________。
(3)流程二中,加入烧碱溶解SiO2的化学方程式为_________。
(4)滤液⑤中的可溶性盐是NaCl、______(填化学式),滤液⑨与过量氨水反应的离子方程式为_____。
(5)在电解氧化铝制取金属铝的反应中,氧化产物与还原产物的质量之比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com