
【题目】关于有机物的正确叙述是( )
A.CH4O与C3H8O一定是同系物
B.同分异构体一定具有相似的化学性质
C.完全燃烧等质量的苯与苯乙烯,耗氧量相同
D.向溴乙烷中滴加硝酸银溶液,产生黄色沉淀
科目:高中化学 来源: 题型:
【题目】Fe(OH)3胶体与FeCl3溶液共同的性质是( )
A. 两者都有丁达尔效应
B. Fe(OH)3胶体是红褐色沉淀
C. 两者都能透过滤纸
D. 都很稳定,其中Fe(OH)3胶体比FeCl3溶液更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.1mol苯乙烯( ![]() )中含有的C=C数为4NA
)中含有的C=C数为4NA
B.标准状况下,2.24L己烷含有的分子数为0.1NA
C.1mol甲基含10NA个电子
D.某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列表格
物质 | N2 | HNO3 | SO2 |
质量/g | ___ | 18.9 | ___ |
物质的量/mol | ___ | ___ | 1.5 |
标况下的体积/L | 4.48 | ___ | ___ |
分子个数 | ___ | ___ | ___ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向25mL 0.1molL﹣1 MOH 溶液中逐滴加入0.2molL﹣1 HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: 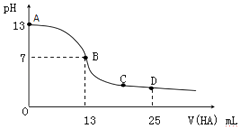
(1)MOH与HA恰好完全反应时,溶液呈性(填“酸”、“碱”或“中”),用离子方程式表示其原因 . 此时,混合溶液中由水电离出的c(H+)0.2mol.L﹣1 HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(2)D点时,溶液中c(A﹣)+c(HA)2c(M+)(填“>”“<”或“=”);若此时测得混合溶液的pH=3,则 c(HA)+c(H+)=molL﹣1(数字表达式,不必具体算出结果).
(3)分别写出C点混合溶液中各离子浓度的大小关系 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物的分离方法不可行的是
A.沸点不同的液态混合物可用蒸馏方法分离
B.互不相溶的液态混合物可用分液方法分离
C.互溶的液态混合物可用萃取的方法分离
D.可溶于水的固体与难溶于水的固体形成的混合物可用溶解、过滤、蒸发的方法分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应是铝的一个重要性质.某校化学兴趣小组同学为了克服传统铝热反应纸漏斗易燃烧,火星四射等缺点,将实脸改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后补到“铁块”混合物.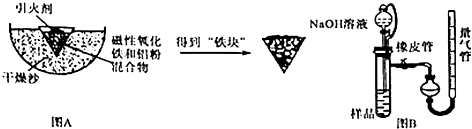
(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是 .
(2)该铝热反应的化学方程式为 .
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气体体积以测量样品中残留铝的百分含量.试回答下列问题:①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为 .
②量气管在读数时必须进行的步骤是 .
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为 .
④装置中分液漏斗上端和烧瓶用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用.如果装置没有橡胶管,测出铝的百分含量将会(填“偏大”或“偏小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠具有很活泼的化学性质,易与很多物质反应。钠与水的反应(水中滴有酚酞溶液)实验现象和结论如下表,请同学们完成填空。
实验现象 | 解释与结论 |
(1) _______________ | 密度比水小 |
(2)熔化成闪亮的小球 | _______________ |
(3)四处游动、嘶嘶作响 | _______________ |
(4)反应后溶液呈红色 | _______________ |
(5)钠与水反应方程式是__________________。实验室中金属钠通常保存在_______。
(6)实验室常用氢氧化钠溶液来吸收多余的氯气以防止污染空气,请写出发生反应的方程式_______________。漂白粉长时期露置在空气中会失效,用方程式表示其失效的原因_________________________;______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是( )
A.反应后溶液中Fe3+物质的量为0.8mol
B.反应后产生13.44L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol
D.由于氧化性Fe3+>H+ , 故反应中先没有气体产生后产生气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com