
【题目】在烃的分子结构中,每减少2个氢原子,则碳碳间便增加一对共用电子。已知分子组成为CnH2n+2 的烃分子中碳碳间的共用电子对数为 n-1,则化学式为CnH2n-2 的烃分子结构中,碳碳间的共用电子对数为 ,Cx 也可视为烃脱氢后的产物,则C60 中碳碳间的共用电子对数为 ;若某碳单质分子中碳碳间的共用电子对数为 140 ,则该单质的分子式为 。
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图(如图),电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
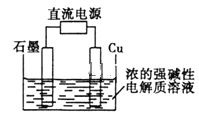
A. 电子的流向:电源负极→石墨电极→Cu→电源正极
B. 铜电极上的电极方程式为2Cu+H2O-2e-=Cu2O+2H+
C. 电解后溶液的pH变大
D. 当有0.1mol电子转移时,有0.1mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )
A. ![]() mol·L-1B.
mol·L-1B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1D.
mol·L-1D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种试剂中:①浓溴水②食盐溶液③浓H2SO4④Na2SO3溶液⑤石灰水⑥氢硫酸 ⑦NaClO溶液,长期放置在空气中不容易变质而浓度变小的组合是 ( )
A.①③④B.④⑤⑥C.②④⑦D.只有①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列数量的各物质所含原子数按由大到小的顺序排列是________。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________L。
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写方程式
(1)过氧化钠与CO2反应的化学方程式:___;
(2)将少量硫酸铝溶液滴入足量氨水中的离子方程式:___;
(3)铁与水蒸气反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如图工艺流程:

请回答下列问题:
(1)沉淀B的成分是____(填化学式,下同);
(2)沉淀C的成分是___;
(3)沉淀F转化为物质M的化学方程式为___;
(4)溶液A与过量烧碱反应生成沉淀C的离子方程式____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列环境问题与所对应的物质不相关的是( )
A. 温室效应——二氧化碳B. 光化学烟雾——二氧化氮
C. 酸 雨——二氧化硫D. 臭氧层破坏——一氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点232℃)与Cl2反应制备SnCl4,装置如图。

已知:①SnCl2、SnCl4有关物理性质:

②SnCl4极易水解生成SnO2·xH2O。
回答下列问题:
(1)导管a的作用是_________________________________,装置A中发生反应的离子方程式为____________________。
(2)当观察到装置F液面上方___________时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是①_________________________________;②____________。
(3)若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应化学方程式为_________________________________。
(4)Cl2和锡的反应产物有SnCl4和SnCl2,为防止产品中带入过多的SnCl2,可采取的措施是____________________________________________。
(5)滴定分析产品中2价Sn(Ⅱ)的含量:用分析天平称取5.000g产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用0.1000mol·L-1的碘标准溶液滴定至终点时消耗20.00mL,则产品中Sn(Ⅱ)的含量为___________。(已知Sn2++I2=2I-+Sn4+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com