
【题目】羟胺的电离方程式为:NH2OH+H2O![]() NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL 0.lmol/L羟胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL 0.lmol/L羟胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
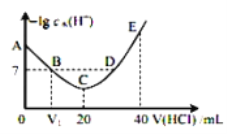
A.图中V1<10
B.A点对应溶液的pH=9.5
C.A、B、C、D四点中酸性最强的点为D点
D.E点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+c(NH2OH)
【答案】D
【解析】
A.羟胺是一元弱碱,若V1=10,则反应恰好起始时产生等量的NH2OH和NH3OH+,NH3OH+的水解常数![]() =1.1×10-5比NH2OH电离常数9.0×10-9大,溶液呈酸性,B点时水的电离达到10-7mol/L,则羟胺过量,需要少滴加一部分HCl,所以V1应<10,故A正确;
=1.1×10-5比NH2OH电离常数9.0×10-9大,溶液呈酸性,B点时水的电离达到10-7mol/L,则羟胺过量,需要少滴加一部分HCl,所以V1应<10,故A正确;
B.羟胺的电离方程式为:NH2OH+H2ONH3OH++OH-,已知25℃时,其电离平衡常数为Kb=9.0×l0-9,起始浓度为c0=0.1mol/L,溶液中c(OH-)=![]() =
=![]() =3.0×10-5mol/L,c(OH-)=
=3.0×10-5mol/L,c(OH-)=![]() mol/L=
mol/L=![]() ×10-9mol/L,pH=-lg
×10-9mol/L,pH=-lg![]() ×10-9mol=9+lg3=9.5,故B正确;
×10-9mol=9+lg3=9.5,故B正确;
C.C点溶液中水电离生成的氢离子最大,则C点盐酸与羟胺恰好完全反应产生NH3OHCl,C点以后HCl过量,所以D点酸性最强,溶液呈酸性,故C正确;
D.E点时加入HCl的体积为40mL,根据电荷守恒:c(H+)+c(NH3OH+)=c(OH-)+c(Cl-),根据物料守恒:2c(NH3OH+)+2c(NH2OH)=c(Cl-),则有c(H+)=c(OH-)+c(NH3OH+)+2c(NH2OH),故D错误;
故答案为D。


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.1mol钠蒸气与2mol钠蒸气完全燃烧时,燃烧热相同
B.燃烧热是反应热的种类之一
C.在稀溶液中:H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
D.在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)![]() 2H2O(l) ΔH=+285.8kJ·mol1
2H2O(l) ΔH=+285.8kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃,101kPa下,lg C8H18(辛烷)(相对分子质量:114)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ·mol-1
B. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ·mol-1
C. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=+5518kJ·mol-1
D. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-48.40kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)若电解饱和食盐水时消耗117gNaCl,则理论上最多可得到___L(标准状况)氯气。
(2)为测定K2SO4溶液的浓度,取25.00mL待测液,向其中加入过量BaCl2溶液,充分反应后过滤并干燥,得到白色沉淀的质量是1.165g。该K2SO4溶液的物质的量浓度是多少?___(写出具体的计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入NO2,发生反应2NO2(g)![]() N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
t/℃ | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
下列说法不正确的是( )
A.27℃,该平衡体系中的NO2转化率为![]()
B.平衡时,NO2的消耗速率为N2O4消耗速率的2 倍
C.室温时,将盛有NO2的密闭玻璃球放入冰水中其颜色会变浅
D.其他条件不变,增大NO2起始量,平衡正移,该反应的化学平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)古代的“药金”外观与金相似,常被误认为是金子。其冶炼方法如下:将碳酸锌、赤铜(Cu2O)、木炭按一定比例混合加热到800℃,即得金光闪闪的“药金”。
①“药金”的主要成分是__(填化学式)。
②有关冶炼的化学方程式是__。
(2)某地出产的孔雀石的主要成分是Cu2(OH)2CO3。
①试写出该孔雀石在加热条件下分解的化学方程式:__。
②试以①中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方法制取金属铜。供选择的试剂有木炭、铁屑、生石灰、稀硫酸,不得另选其他试剂。写出两种方法制取金属铜的化学方程式。
a.湿法冶炼:__、__(可不填满,也可补充,下同)。
b.高温冶炼:__。
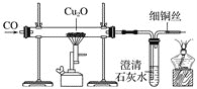
(3)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。实验室可用如图所示装置进行实验,当硬质玻璃管中的反应结束时,应进行的实验操作是___。
(4)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,完全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。结合质量守恒定律,推断这种铜的氧化物的化学式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为__。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
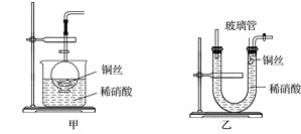
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是__(填字母)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是__。
②让反应停止的操作方法及原因是__。
(4)以下收集NO气体的装置,合理的是__(填字母)。
A. B.
B.![]() C.
C. D.
D.![]() E.
E.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

(1)B装置中的干燥剂是_____(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1--2滴浓盐酸,可观察到E装置中的现象是产生______(填”烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____(填“a”“b”或“c”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com