
【题目】下列混合物能用分液法分离的是 ( )
A. 果糖与乙醚 B. 苯和溴苯
C. 乙酸乙酯和Na2CO3溶液 D. 葡萄糖与果糖混合液
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】某课外小组准备在实验室配制100mL1.0mol·L-1的硝酸溶液,然后再研究金属铜与硝酸的反应情况。
(1)配制100mL1.0mol·L-1的硝酸溶液,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需要的玻璃仪器是______________________。
(2)若用10 mol·L-1的浓硝酸来配制上述溶液,需要量取浓硝酸的体积是_______mL。
(3)配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是__________。
A.定容摇匀后发现液面低于刻度线,再加水至刻度线
B.定容时俯视容量瓶的刻度线
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就进行定容操作
D.容量瓶用蒸馏水洗涤后未烘干
(4)课外小组同学将制得的硝酸与铜片在下列装置中反应,反应初期观察到大试管中的液体a逐渐变为蓝色,试管上方有浅红棕色气体出现。
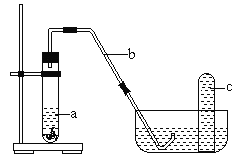
① 反应初期液体a逐渐变为蓝色是由于反应生成了____________(填化学式)。
② 导致红棕色气体在试管c中颜色消失的反应方程式为____________________。
③ 你能否通过该实验初期现象得出1.0mol·L-1的硝酸与铜片反应直接生成红棕色NO2的结论?_________(填“能”或“不能”),理由是 __________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期元素.B、E同主族,且满足最高正化合价+最低负化合价=0;A与C、D与C之间都能形成原子个数比分别为2:1和1:1的两种化合物.试解答下列有关问题.
(1)在A2C 2分子中含有的化学键是______和______.
(2)C与D形成的化合物的电子式为______.
(3)实验室可用由B、C、D组成的化合物为反应物之一制取由A、C、D组成的化合物,反应的化学方程式为______.
(4)写出E单质与A、C、D形成的化合物的水溶液反应的离子方程式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学的最大特点在于它是在始端就采用实现污染预防的科学手段,因而过程和终端均为零排放或零污染。绿色化学主张在通过化学转换获取新物质的过程中充分利用每个原子,具有“原子经济性”,因此它既能够充分利用资源,又能够防止污染。下列化学反应,不符合绿色化学概念的是( )
A. 消除硫酸厂尾气排放:SO2+NH3+H2O=(NH4)2SO3
B. 制CuSO4:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
C. 消除制硝酸工业尾气的氮氧化物污染:NO2+NO+NaOH=2NaNO2+H2O
D. 制CuSO4:2Cu+O2=2CuO, CuO+H2SO4(稀)=CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是_____________(填序号)
A.亚硫酸溶液加入Na2CO3溶液中,产生气泡
B.氧化性:浓H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为—2价
D.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
① 羰基硫的结构式为:________________。沸点:CO2_________COS(填“大于”或“小于”),说明原因_____________________。
②下列有关羰基硫的推测肯定不正确的是_________________
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③ 羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为________;气体单质a为____________________.
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)![]() COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是__________________反应(填“放热”或“吸热”)。
②平衡时,继续通入CO10mol和H2S10mol,一段时间后再次达到平衡,此时H2S的转化率_____(填“增大”“减小”或“不变”)
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是____________
A.容器内气体密度保持不变
B.CO、H2S、COS、H2的浓度均不再变化
C.c(H2)=c(H2S)
D.v(H2)正=v(H2S)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用化学方程式解释下列现象:
①硝酸久置成黄色的原因:___________________________________________
②氨气溶于水使无色酚酞变红的原因: _____________________________________
(2)铁粉与过量的稀硝酸常温下可以发生如下反应:
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
当铁粉过量时,在标准状况下反应生成2.24LNO气体,反应后溶液的溶质为________,则一共有______g铁参加反应,被还原的HNO3与未被还原的硝酸物质的量之比等于______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图中的曲线是表示其他条件一定时,2NO+O2![]() 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是

A. a点 B. b点 C. c点 D. d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED系列产品是被看好的一类节能新产品,下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是
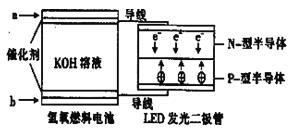
A.a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O
B.b处通入氧气,为电池的正极
C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半导体连接的是电池负极.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,1.01×105Pa时,反应:2N2O5(g) = 4NO2(g) +O2(g) △H = + 56.76 kJ·mol-1,能自发进行的原因是
A. 是吸热反应 B. 是放热反应 C. 是熵减少的反应 D. 熵增大效应大于能量效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com