
【题目】某烷烃的结构简式是CH3CH2CH2CH(CH2CH3)CH3,它的正确命名是
A. 3-甲基己烷 B. 2-乙基戊烷 C. 4-乙基戊烷 D. 2,2-二甲基戊烷
 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关维生素的说法中不正确的是
A.维生素是参与生物生长发育和新陈代谢所必需的一类高分子化合物
B.维生素C溶于水,溶液显酸性
C.生吃新鲜蔬菜要比熟吃时维生素C的损失小
D.含维生素C能使蓝色的碘的淀粉溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知常温下,H2SO3的电离常数为Kal=1.54×10-2,Ka2=1.02×10-7,H2CO3的电离常数为Kal=4.30×10-7,Ka2=5.60×10-11。
(1)下列微粒可以大量共存的是________(填字母)。
a.CO![]() 、HSO
、HSO![]() b.HCO
b.HCO![]() 、HSO
、HSO![]()
c.SO![]() 、HCO
、HCO![]() d.H2SO3、HCO
d.H2SO3、HCO![]()
(2)已知NaHSO3溶液显酸性,解释原因:_____________________________;
NaHSO3的稀溶液中各离子浓度从大到小的排列顺序是_____________________________。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO![]() 、CO
、CO![]() 、HSO
、HSO![]() 、HCO
、HCO![]() 浓度从大到小的顺序为____________________________。
浓度从大到小的顺序为____________________________。
(4)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_______________________。
Ⅱ.Na2S2O5(焦亚硫酸钠)是常见的食品抗氧化剂之一。
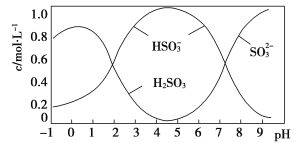
(5)将0.5 mol Na2S2O5溶于水配成1 L溶液,该溶液pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化情况如图所示。写出Na2S2O5溶于水的化学方程式:____________________________;当溶液pH小于1后,溶液中H2SO3的浓度变小,其原因可能是________________________。pH=3时,溶液中主要含硫粒子浓度的大小关系为________。
(6)已知:Ksp(BaSO4)=1.0×10-10,Ksp(BaSO3)=5.0×10-7。将部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO![]() 沉淀完全[c(SO
沉淀完全[c(SO![]() )≤1.0×10-5mol·L-1],此时溶液中c(SO
)≤1.0×10-5mol·L-1],此时溶液中c(SO![]() )≤________mol·L-1。
)≤________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,2 mol X2(气)和6 mol Y2(气)化合生成4 mol的气体化合物,则该气体化合物的化学式为
A.XY3 B.XY C.X3Y D.X2Y3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是
A.在常温常压下,11.2 LN2含有的分子数为0.5 NA
B.71gCl2所含原子数为NA
C.在常温常压下,1molNe含有的原子数为NA
D.在同温、同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 (1)写出该反应的平衡常数表达式:K= 。
(1)写出该反应的平衡常数表达式:K= 。
已知:![]() >
>![]() ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2浓度的变化的曲线是 。

用O2表示从0—2s内该反应的平均速率υ(O2)= 。
(3)能说明该反应已达到平衡状态的是 。
a.C(NO2)=2C(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4) 为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能源的说法不正确的是
A. 煤的干馏是物理变化,煤的气化和液化是化学变化
B. 煤油可由石油分馏获得,可用作燃料和保存少量金属钠
C. 沼气(主要成分是CH4)是可再生能源
D. 太阳能、氢能、风能、地热能、生物质能都是新能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将250 mL含BaCl2和KCl的混合溶液分成10等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则原混合溶液中钾离子物质的量浓度为
A.4(b-2a)mol/L B.20(2a-b)mol/L
C.20(b-2a)mol/L D.40(b-2a)mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com