
 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中已铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中已铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )| A、阳极电极方程式为Al-3e+6OH-=Al2O3+H2O |
| B、随着电解的进行,溶液的PH逐渐增大 |
| C、当阴极生成气体3.36L(标况)时,阳极增重2.4g |
| D、电解过程中H+移向Al电极 |
| ||
| ||
| 3.36L |
| 22.4L/mol |


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水的浓度等于盐酸的浓度 |
| B、原氨水中有1%的含氮微粒为NH4+ |
| C、氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D、混合溶液中c(NH4+)+c(NH3?H2O)+c(NH3)=5×10-4mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ |
| B、向无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀出现,则溶液中含有SO42ˉ |
| C、向某溶液中滴加少量氯水,再滴加KSCN溶液,若溶液变成血红色,则原溶液中一定有Fe2+ |
| D、向某黄色溶液中加入淀粉溶液,若溶液变蓝色,则原溶液中含有I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3种 | B、4种 | C、5种 | D、6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
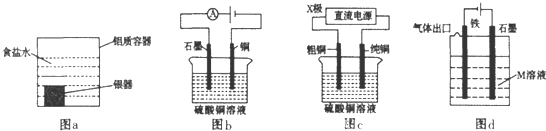
| A、利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-=2Ag+S2- |
| B、图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出 |
| C、图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D、图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、减小容器体积,平衡不移动 |
| B、加入催化剂,B的转化率增大 |
| C、增大c(A),A的转化率增大 |
| D、降低温度,v正增大,v逆减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 仔细观察下面两种电池的构造示意图,完成下列问题:
仔细观察下面两种电池的构造示意图,完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述 | 原因或解释 |
| A | SO2通入氢氧化钠酚酞溶液中,溶液褪色 | SO2具有漂白作用 |
| B | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| C | 过滤时应用玻璃棒引流和搅拌 | 防止滤液溅出和缩短过滤时间 |
| D | 浓硝酸应保存在棕色瓶中 | 浓硝酸易挥发 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com