
����Ŀ�������ֶ�����Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���±�������

����ݱ�����Ϣ��д��
��1��Aԭ�ӵĺ�������Ų�ʽΪ________________��
��2��BԪ�������ڱ��е�λ����____�����Ӱ뾶��B_____A(��������������С����)��
��3��Cԭ�ӵĵ����Ų�ͼ��________����ԭ�Ӻ�����________��δ�ɶԵ��ӣ�������ߵĵ���Ϊ________����ϵĵ��ӣ�������________�Ρ�
��4��Dԭ�ӵ���Χ�����Ų�ʽΪ____________��D���Ľṹʾ��ͼ��____________��
��5��B������������Ӧ��ˮ������A������������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽΪ________��B������������Ӧ��ˮ������D���⻯���ˮ��Һ��Ӧ�Ļ�ѧ����ʽΪ__________________��
���𰸡���1��1s22s22p63s1
��2����3���ڵ���A�� С��
��3��![]() 3 p �Ĵ�
3 p �Ĵ�
��4�� 3s23p5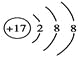
��5��NaOH��Al(OH)3===NaAlO2��2H2O 3HCl��Al(OH)3===AlCl3��3H2O
������������������Ƕ�������(��ϡ��������)ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ���A��Na��B��Aͬ���ڣ�������������ˮ��������ԣ�B��Al��Ԫ�ص���̬�⻯�K������ˮ���������������C��N���Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ����ˮ���������г��õ�����ɱ������D��Cl��
��1�� Naԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s1��
��2�� AlԪ�������ڱ��е�λ���ǵ�3���ڵ���A�壻���Ӱ뾶��BС��A��
��3��Nԭ�ӵĵ����Ų�ͼ��![]() ����ԭ�Ӻ�����3��δ�ɶԵ��ӣ�������ߵĵ���Ϊp����ϵĵ��ӣ������ʷĴ��Ρ�
����ԭ�Ӻ�����3��δ�ɶԵ��ӣ�������ߵĵ���Ϊp����ϵĵ��ӣ������ʷĴ��Ρ�
��4�� Clԭ�ӵ���Χ�����Ų�ʽΪ3s23p5��D���Ľṹʾ��ͼ��![]() ��
��
��5����������������������Ӧ�Ļ�ѧ����ʽΪ)NaOH��Al(OH)3===NaAlO2��2H2O�������������ᷴӦ�Ļ�ѧ����ʽΪ3HCl��Al(OH)3===AlCl3��3H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����������������ǻ�����һ����Ҫ����������Ӧ�úʹ������Ļ����������������������Ҫ�����塣
(1)��֪��N2(g)+O2(g)=2NO(g) ��H=+181.5 kJ��mol��1ij����С�鳢�����ù����������ս���NO�ķֽ⡣������� ����� �������![]() �ֱ��ʾN2 ��NO��O2����������ڹ����������ֽ�NO�Ĺ�������ͼ��ʾ���������������Ĺ����У�����״̬��͵���___________(����ĸ���)��
�ֱ��ʾN2 ��NO��O2����������ڹ����������ֽ�NO�Ĺ�������ͼ��ʾ���������������Ĺ����У�����״̬��͵���___________(����ĸ���)��

(2)Ϊ��������β����NOx���ŷţ�������CxHy(��)����ԭNOx���������������Ⱦ��
���磺��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1=��574 kJ/mol
��CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) ��H2=��1160 kJ/mol
��CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ��H3
���H3=___________��
(3)��������(ClNO)���л��ϳ��г����Լ�����֪��2NO(g)+Cl2(g)![]() 2 ClNO(g) ��H��0
2 ClNO(g) ��H��0
��һ���¶��£���2 molNO��2 molCl2����2L�ܱ������з�����Ӧ�����÷�Ӧ4min���ƽ�⣬��ʱѹǿ�dz�ʼ��0.8������ƽ����Ӧ����v(Cl2)=___________mol��L��1��min��1�����п��жϷ�Ӧ��ƽ��״̬����___________(�������ĸ)��
A ��������ƽ����Է�����������
B ��������ܶȱ��ֲ���
C NO��Cl2�����ʵ���֮�ȱ��ֲ���
D ÿ����1 moI NOͬʱ����1molClNO
��Ϊ�˼ӿ컯ѧ��Ӧ���ʣ�ͬʱ���NO��ת���ʣ�������������ʱ���ɲ�ȡ�Ĵ�ʩ��___________(��ѡ�������ĸ)��
A �����¶� B ��С�������
C �ٳ���Cl2���� D ʹ�ú��ʵĴ���
��һ���������ں��º��ݵ��ܱ������У���һ����������NO(g)��Cl2(g)��ƽ��ʱClNO�����������n(NO)/n(Cl2)�ı仯ͼ����ͼ(b)��ʾ����n(NO)/n(Cl2)=2.5ʱ���ﵽƽ��״̬��ClNO���������������ͼ��D��E��F�����е�___________�㡣

(4)��֪2NO(g)+O2(g)![]() 2NO2(g)�ķ�Ӧ���̷�������
2NO2(g)�ķ�Ӧ���̷�������
��2NO(g)![]() N2O2(g)(��)��v1��=k1��c2(NO)��v1�� =k1��c (N2O2)
N2O2(g)(��)��v1��=k1��c2(NO)��v1�� =k1��c (N2O2)
��N2O2(g)+O2(g)![]() 2NO2(g)(��)��v2��=k2��c(N2O2)��c(O2)��v2��=k2��c2(NO2)
2NO2(g)(��)��v2��=k2��c(N2O2)��c(O2)��v2��=k2��c2(NO2)
�ȽϷ�Ӧ�ٵĻ��E1�뷴Ӧ�ڵĻ��E2�Ĵ�С��E1___________E2(����>����"<������=��)��2NO(g)+O2(g)![]() 2NO2(g)��ƽ�ⳣ��K��������Ӧ���ʳ���k1����k1����k2����k2���Ĺ�ϵʽΪ___________��
2NO2(g)��ƽ�ⳣ��K��������Ӧ���ʳ���k1����k1����k2����k2���Ĺ�ϵʽΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ֱ���0.1 mol��L��1��Һ��������ʵ�飬��������ȷ����
A. ��NaHCO3��Һ��ͨCO2��pH=7��c(Na+) = c(HCO3-) +2c(CO32-)
B. ��CH3COONa��Һ�м����Ũ�ȵ���������c(Na+)=c(Cl![]() )
)
C. ��NaHSO4��Һ�м����Ũ�ȵ������Ba(OH)2��Һ��pH=13
D. ��ˮ�м�������NH4Cl���壺![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ������£�NCl3��һ����״Һ�壬����ӿռ乹����NH3���ƣ����ж�NCl3��NH3���й�������ȷ����( )
A. ������N��Cl��������CCl4������C��Cl���������
B. �ڰ�ˮ�У���NH3��H2O�����(�á�������ʾ)����γ�NH3��H2O���ӣ���NH3��H2O�ĽṹʽΪ��
C. NCl3�����ǷǼ��Է���
D. NBr3��NCl3�ӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ����仯ʱ�����˷������Ӽ��������ͬ�����͵���(����)
A. ����ɱ��ֱ����ȱ�Ϊ����
B. �����������ֱ����ȱ�Ϊ����
C. �Ȼ������Ȼ���ֱ��ܽ���ˮ��
D. ����������ֱ������ۻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ��� K+��NH4+��Ca2+��Cl�C��SO42�C��CO32�C�е������֡�Ϊ��ȷ������Һ����ɣ�ȡ100mL������Һ����������ʵ�飺(�����Լ�������������ȫ���ݳ�)����˵������ȷ����

A. ԭ��Һ��һ������SO42�C��CO32�C��NH4+
B. ԭ��Һ��һ��������Ca2+�����ж�Cl�C�Ƿ����
C. Ҫȷ��Cl�C�Ƿ���ڣ���ȡ������Һ2������������ϡ�������
D. ԭ��Һ�� c(K+ )��0.1 mol�� L�� 1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ij����С�齫��ͼ��ʾװ�ð�һ��˳�����ӣ���ʵ��������ȡһ������FeCl3����ͨ�����������ַ�Ӧ������ش��������⣺
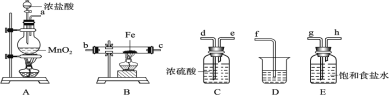
��1��A �з�����Ӧ�Ļ�ѧ����ʽΪ________________________���ڸ÷�Ӧ�е� 0.4molHCl������Ӧʱ�����ɱ�״���µ�Cl2 �����Ϊ______��Ũ�����ڷ�Ӧ����ʾ������������__������ţ���
A��ֻ�л�ԭ�� B����ԭ�Ժ����� C��ֻ�������� D�������Ժ�����
��2����װ�õ���ȷ����˳��Ϊ����дװ�ô��ţ�A��_____��_____��_____��D��
��3��װ�� E ��������_______��д��װ�� D(D����ʢ��ҺΪ NaOH)�з�Ӧ�Ļ�ѧ����ʽ_______
��4����ҵ���õ�ⷨ�Ʊ������Ļ�ѧ����ʽΪ��____________��
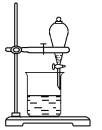
��ijС����CCl4��ȡ��ˮ�еĵ⣬����ͼ�ķ�Һ©���У��²�Һ���__________ɫ�����Ǵ�Һ©��������ȴδ��Һ�����£�ԭ�������__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϡ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H2
CH3OH��g��+H2O(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3
CO(g)+H2O(g) ��H3
��1����֪��Ӧ���е���صĻ�ѧ�������������£�
��ѧ�� | H��H | C��O | C��O | H��O | C��H |
E/(kJ��mol-1) | 436 | 343 | 1076 | 465 | 413 |
�ɴ˼����H1=__________kJ��mol-1����֪��H2=-58kJ��mol-1�����H3=_________kJ��mol-1
��2����Ӧ�ٵĻ�ѧƽ�ⳣ��K�ı���ʽΪ_______________���۵Ļ�ѧƽ�ⳣ��K�ı���ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ�����������缫����һ�����ı���Na2SO4��Һ�н��е�⣬ͨ��һ��ʱ����������ݳ�a mol���壬ͬʱ����w��Na2SO4��10H2O���壬���¶Ȳ��䣬��ʱʣ����Һ������������
A. ![]() ��100% B.
��100% B. ![]() ��100%
��100%
C. ![]() ��100% D.
��100% D. ![]() ��100%
��100%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com