
【题目】氢化阿托醛  是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:

请根据上述合成路线,回答下列问题:
(1)氢化阿托醛所含官能团的名称为_____________;一定条件下,1 mol氢化阿托醛最多可跟______mol氢气加成。
(2)②的反应类型是__________________。写出它的化学方程式:_____________。
(3)④中所用试剂X为____________。
(4)写出反应⑤的化学方程式:_______________________。
【答案】 醛基 4 消去反应 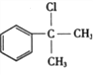 +NaOH
+NaOH![]()
![]() +NaCl+H2O 氢氧化钠溶液 2
+NaCl+H2O 氢氧化钠溶液 2![]() +O2→2
+O2→2![]() +2H2O
+2H2O
【解析】根据题中各物质的转化关系,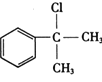 在氢氧化钠醇溶液中发生消去反应生成A为
在氢氧化钠醇溶液中发生消去反应生成A为![]() ,A与溴化氢在双氧水条件下发生信息中的反应生成B为
,A与溴化氢在双氧水条件下发生信息中的反应生成B为![]() ,B在氢氧化钠水溶液中发生水解生成C为
,B在氢氧化钠水溶液中发生水解生成C为![]() ,C发生氧化反应生成氢化阿托醛(
,C发生氧化反应生成氢化阿托醛(![]() )。
)。
(1)根据氢化阿托醛的结构简式可知,所含官能团的名称为醛基,由于氢化阿托醛中有一个苯环和一个醛基,所以一定条件下,1mol氢化阿托醛最多可跟4mol氢气加成,故答案为:醛基;4;
(2)反应②为 在氢氧化钠醇溶液中发生消去反应生成
在氢氧化钠醇溶液中发生消去反应生成![]() ,反应的方程式为
,反应的方程式为 +NaOH
+NaOH![]()
![]() +NaCl+H2O,故答案为:消去反应;
+NaCl+H2O,故答案为:消去反应; +NaOH
+NaOH![]()
![]() +NaCl+H2O;
+NaCl+H2O;
(3)根据上面分析可知,④中所用试剂X为氢氧化钠溶液,故答案为:氢氧化钠溶液;
(4)C为![]() ,C发生氧化反应生成氢化阿托醛(
,C发生氧化反应生成氢化阿托醛(![]() ) ,反应的方程式为:2
) ,反应的方程式为:2![]() +O2→2
+O2→2![]() +2H2O,故答案为:2
+2H2O,故答案为:2![]() +O2→2
+O2→2![]() +2H2O。
+2H2O。


科目:高中化学 来源: 题型:
【题目】如图所示为实验室某浓盐酸试剂瓶上标签的有关内容。取该盐酸10mL,加蒸馏水稀释至250mL,向其中加入mg锌粉恰好完全反应。
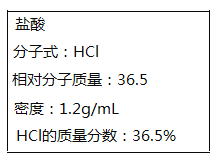
(1)写出锌粉与盐酸反应的离子方程式______________。
(2)求原浓盐酸的物质的量浓度c=____________。
(3)计算出m=___________。
(4)反应中生成的H2可以和标准状况下______mL的O2恰好完全反应。
(5)向反应后的溶液中加入0.6mol/L的AgNO3溶液至不再产生沉淀,共消耗VmL AgNO3溶液,则V的值是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列关于电解质溶液的说法不正确的是
A. 加水稀释Na2S溶液过程中,水电离出的c(H+) c(OH-)逐渐减小
B. pH=5的NH4Cl溶液,用蒸馏水稀释10倍后,溶液的pH<6
C. pH=2的一元酸HA溶液与pH=12的NaOH溶液等体积混合后,c(Na+)<c(A-)
D. pH相同的①NH4Cl、②NH4Al(SO4)2、③(NH4)2SO4三种溶液中c(NH![]() ):①=③>②
):①=③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用下图所示的装置,用环己醇制备环己烯。
已知: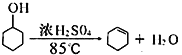
相对分子质量 | 密度/g cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 82 | 0.81 | -103 | 83 | 难溶于水 |
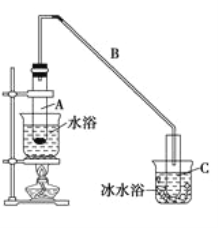
(1)制备粗品
将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为______________________。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______________________________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在_______层(填“上”或“下”),分液后用________(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是_______________,实验中冷却水从______(填字母)口进入。蒸馏时要加入生石灰,目的是__________________________。
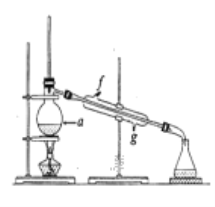
(3)若在制备粗品时环已醇随产品一起蒸出,则实验制得的环己烯精品质量_______(填“高于”、“ 低于”)理论产量。本实验所得到的环已烯质量为6.5g,则产率是______(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述中正确的是
A. 标准状况下,2.24 LCCl4中含有的氯原子数为0.4NA
B. 常温常压下,36g等体积混合的CO与CO2混合气体中含有的氧原子数为1.5NA
C. 1molFe与足量氯气反应时转移的电子数为2NA
D. 1L1mol·L-l的NaClO溶液中含有ClO-的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A:
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%
②下图是该有机物的质谱图,
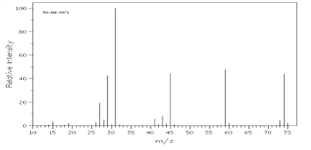
③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰。
④A的核磁共振氢谱有两个峰。
请回答:
(1)A的实验式(最简式)为________,相对分子质量为_______,分子式为_____________。
(2)已知A的最简式能否确定A的分子式(填“能”或“不能”)______,为什么_______。
(3)A的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨的反应为N2+3H2![]() 2NH3+Q。下表是某次反应时NH3的浓度变化:
2NH3+Q。下表是某次反应时NH3的浓度变化:
时间(min) | 0 | 5 | 10 | 15 | 20 |
c(NH3)(mol/L) | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
完成下列填空:
(1)由表中数据计算0~10 min时,用H2表示的平均反应速率为________________。降低温度,反应的平衡常数将______________(填“增大”、“减小”或“不变”)。若要增大反应速率且提高H2利用率,可采取的措施有________________。
(2)若反应中气体混合物的密度保持不变,能否说明该反应已经达到平衡状态?并说明理由。____________________________________________________________________
(3)用右图所示装置进行有关氨气性质的实验,挤出胶头滴管中的水,打开止水夹后的实验现象是_____________。

(4)氨气溶于水后溶液显碱性的原因是(用方程式表示)____________________________________________。若在氨水中逐滴滴加盐酸,则溶液的pH将__________(填“增大”、“减小”或“不变”);当恰好完全反应时,则c(NH4+)________c(Cl-)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实践中可根据核磁共振氢谱(PMR)上观察到氢原子给出的峰值情况,确定有机物的结构。现在将有机物A 0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。则:
(1)此有机物的化学式为:_______________________________.
(2)已知此有机物含有苯环,在PMR谱上峰给出的稳定强度出现了五组峰,如图所示。请据图写出此有机物A的结构简式:__________________________.
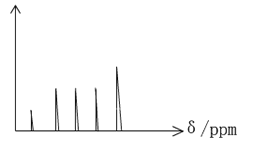
(3)请写出此有机物A在Ni的催化作用下与H2加成反应的化学方程式:________________.
(4)请写出此有机物A在浓H2SO4催化作用下与浓HNO3发生间位取代反应的化学方程式:_________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com