
| A. | 反应①是置换反应,HCl表现还原性 | |
| B. | 反应②是复分解反应,HCl表现氧化性 | |
| C. | 反应③中HCl既有氧化性也有还原性 | |
| D. | 反应①中氧化剂和氧化产物的物质的量之比是1:1 |
分析 ①为置换反应,反应中HCl的H元素的化合价降低,Zn元素化合价升高;②为中和反应,元素化合价不变;③2HCl$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑H元素的化合价降低,Cl元素的化合价升高,以此解答该题.
解答 解:A.反应①中HCl的H元素的化合价降低,HCl表现氧化性,故A错误;
B.反应②是复分解反应,元素化合价没有变化,HCl表现酸性,故B错误;
C.2HCl$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑H元素的化合价降低,Cl元素的化合价升高,HCl既有氧化性也有还原性,故C正确;
D.反应①中氧化剂和氧化产物的物质的量之比是2:1,故D错误.
故选C.
点评 本题考查了氧化还原反应,侧重于物质氧化性和还原性判断的考查,明确基本概念内涵是解本题关键,根据元素化合价是否变化来分析解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol化合物 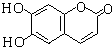 分别与足量的浓溴水、足量的NaOH溶液反应,消耗Br2和NaOH的物质的量相等 分别与足量的浓溴水、足量的NaOH溶液反应,消耗Br2和NaOH的物质的量相等 | |
| B. | 等质量的乙醇、乙烯、甲烷分别充分燃烧,所耗用氧气的量依次减少 | |
| C. | 聚乳酸(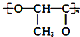 )是由单体之间通过加聚反应合成的 )是由单体之间通过加聚反应合成的 | |
| D. | 实验证实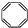 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
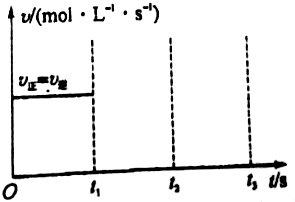 工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.
工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下通入2mol SO2(g)和1mol O2(g)达到平衡时,其反应速率关系如图所示.维持温度、压强不变,在t1时刻充入2mol SO3(g),t2时反应达到新的平衡.请画出t1~t3正、逆反应速率v正、v逆的变化示意图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X原子核外有6个电子层 | B. | X的碳酸正盐不溶于水 | ||
| C. | X的最高化合价为+3价 | D. | X的氢氧化物是一种弱碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| M(OH)n | KSP | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 2.0×10-52 | 3.8 | - |
| Fe(OH)3 | 4.0×10-38 | 1.9 | 3.2 |
| Fe(OH)2 | 8.0×10-16 | 6.95 | 9.95 |
| Ni(OH)2 | 6.5×10-38 | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用SO2漂白过的草帽辫日久会变色 | |
| B. | 硅胶多孔,常用作食品干燥剂和催化剂的载体 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 氯气处理饮用水,在夏季的杀菌效果比在冬季好 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
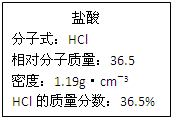 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com