
如图所示的两个实验装置中,溶液的体积均为300mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02 mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
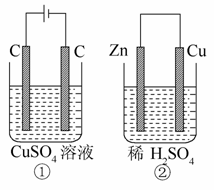
A.溶液的pH变化:①增大,②减小
B.①为原电池,②为电解池
C.电极反应式:①中阳极:4OH--4e-===2H2O+O2↑ ②中负极:2H++2e-===H2↑
D.产生的气体:①0.005 mol,②0.01 mol
科目:高中化学 来源: 题型:
在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)===CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
A.反应物浓度:a点小于c点
B.c点时反应进行的程度最大
C.该反应的正反应为吸热反应
D.Δt1=Δt2时,生成H2的物质的量:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
写出铝单质与强酸、强碱溶液反应的离子方程式,并标出电子转移的方向和数目:________、________。日常生活中接触到的易拉罐有铁质和铝质之分,听装啤酒是铝质易拉罐,向一只充满二氧化碳气体的铝质易拉罐中加入适量的氧氧化钠溶液,并及时堵住,观察到的现象是________,用化学方程式表示产生这一现象的原因是________。若用薄铁质易拉罐做上述实验出现的结果是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,在pH=12的某溶液中,由水电离的c(OH-)为( )
A.1.0×10-7 mol/L
B.1.0×10-6 mol/L
C.1.0×10-4 mol/L
D.1.0×10-12 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶于水的盐在水中存在溶解平衡,例如氯化银在水中的溶解平衡为AgCl(s) Ag++Cl-
Ag++Cl-
在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)·c(Cl-)=1.8×10-10
现把氯化银(足量)分别放入:①100 mL蒸馏水中;②100 mL0.1 mol/L盐酸溶液中;③1 000 mL0.1 mol/L的氯化铝溶液中;④100 mL 0.01 mol/L的氯化镁溶液中,充分搅拌后,相同温度下,银离子浓度由大到小的顺序是(用序号回答)________________________。
在0.1 mol/L氯化铝溶液中,银离子的物质的量浓度最大可达到__________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
甲乙两位同学一起做水果电池的实验,测得数据如下:
| 实验 编号 | 电极 材料 | 水果 品种 | 电极间距/cm | 电压/mV | ||
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
|
|
续表
| 实验 编号 | 电极 材料 | 水果 品种 | 电极间距/cm | 电压/mV | |||
| 2 | 锌 | 铜 | 苹果 | 3 | 650 |
| |
| 3 | 锌 | 铜 | 柑橘 | 3 | 850 |
| |
| 4 | 锌 | 铜 | 西红柿 | 3 | 750 |
| |
| 5 | 锌 | 铝 | 菠萝 | 3 | 650 |
| |
| 6 | 锌 | 铝 | 苹果 | 3 | 450 |
| |
|

甲同学提出的问题,乙同学回答不正确的是( )
| 选项 | 甲同学 | 乙同学 |
| A | 实验5中谁作负极? | 铝作负极 |
| B | 实验1、6电流计指针偏转方向为何不同? | 实验1锌比铜活泼,锌为负极;实验6中铝比锌活泼,铝为负极 |
| C | 水果电池的电压与哪些因素有关? | 只与水果品种有关 |
| D | 仍用上述材料,如何组装一个电压更高的水果电池? | 用铝、铜作电极,菠萝作介质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应:M(g)+N(g)P(g)+Q(g)
ΔH>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol/L,c(N)=2.4 mol/L;达到平衡后,M的转化率为60%,此时N的转化率为__________;
(2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”);
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4 mol/L,c(N)=a mol/L;达到平衡后,c(P)=2 mol/L,a=______。
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=b mol/L;达到平衡后,M的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是六种常见有机化合物分子的球棍模型,下列有关叙述中不正确的是
A.甲、乙、丙属于烃,丁、戊、己属于烃的衍生物
B.丙和己混合后会分层,且丙在上层
C.甲、丙、丁、戊、己均发生取代反应
D.乙和水反应可生成丁,丁和戊反应可生成己

查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或结论正确的是
A.配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水
B.实验室里需要480 mL 2.0 moI·L-1氢氧化钠溶 液,配制溶液时先称量氢氧化钠固38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作
液,配制溶液时先称量氢氧化钠固38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作
C. 25℃时,用惰性电极电解某浓度的NaOH溶液,一小段时间后,NaOH溶液的浓度可能增大,也可能不变
D . K2CO3在酒精灯上灼烧时能直接观察到紫色火焰
. K2CO3在酒精灯上灼烧时能直接观察到紫色火焰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com