
【题目】钡盐生产过程中排出大量钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],某工厂本着资源利用和降低生产成本的目的。在生产BaCO3同时,充分利用钡泥来制取Ba(NO3)2晶体及其它副产品,其部分工艺流程如下:
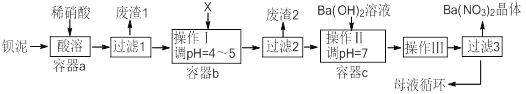
已知: ①Fe(OH)3和Fe(OH)2完全沉淀时溶液的pH分别为3.2和9.7
②Ba(NO3)2在热水中的溶解度大,在冷水中的溶解度小
③Ksp(BaSO4)=1.1×10-10Ksp(BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量饱和的Na2CO3溶液中充分搅拌、过滤、洗涤。用离子方程式说明该提纯的原理 。
(2)上述流程中Ba(FeO2)2与HNO3溶液反应生成两种盐,反应的化学方程式为 。
(3)结合本厂生产实际,X试剂应选下列中的 。
A.BaCl2 | B.BaCO3 | C.Ba(NO3)2 | D.Ba(OH)2 |
(4)废渣2为 。
(5)操作III为 。
(6)过滤III后的母液应循环到容器 中(选填a、b、c) 。
(7)称取w克的晶体样品溶于蒸馏水中加入足量的稀硫酸,反应后经一系列操作称重所得沉淀质量为m克,则该晶体的纯度可表示为______________。
【答案】(1)BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
【不写(s)、(aq)不扣分,写等号不扣分】
(2)Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O 【未配平不给分】
(3)B(4)Fe(OH)3 (5)蒸发浓缩、冷却结晶 【浓缩、结晶即给分】
(6)C(7)261m/(233w)×100% 【不乘以100%也给分】
【解析】试题分析:
(1)根据题目已知信息可知Ksp(BaCO3)>Ksp(BaSO4),BaSO4尽管难溶,也存在一定的溶解度,只要加入足量的饱和Na2CO3溶液,使c(Ba2+)·c(CO32-)>Ksp(BaCO3),就可以发生沉淀的转化,而形成BaCO3沉淀,使BaSO4不断溶解,最后转化为BaCO3,用离子方程式表示为BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq);
BaCO3(s)+SO42-(aq);
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐硝酸钡、硝酸铁,同时产生水,根据质量守恒定律可得该反应的化学方程式为:Ba(FeO2)2+8HNO3 = Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)A、BaCl2可以与硫酸根离子发生沉淀反应,但是不能与H+发生反应,因此不能调节溶液的pH,而且会引入杂质离子Cl-,A错误;B、BaCO3能与H+发生反应,因此能调节溶液的pH,也不引入新的杂质离子,符合题意,B正确;C、Ba(NO3)2不能与H+发生反应,因此不能调节溶液的pH,C错误;D、Ba(OH)2能与H+发生反应,能调节溶液的pH,但是该物质是强碱,制取物质成本高,造价高,不经济,D错误,答案选B;
(4)pH大于3.2时就完全沉淀,所以废渣2为Fe(OH)3。
(5)由于Ba(NO3)2在热水中的溶解度大, 在冷水中的溶解度小,所以操作III为蒸发浓缩、冷却结晶。
(6)过滤3后的母液是析出Ba(NO3)2晶体后的Ba(NO3)2的饱和溶液,为使物质循环利用,根据各个容器中物质的成分可知应循环到容器C中;
(7)Ba(NO3)2晶体溶于水与加入的硫酸溶液发生反应:Ba2++SO42-=BaSO4↓,n(BaSO4)=" m" g÷233g/mol=m/233mol;由于Ba(NO3)2的式量是261,因此w g晶体中含有Ba(NO3)2的质量是m[Ba(NO3)2]= m/233mol×261g/mol=261m/233g,所以该晶体中硝酸钡的质量分数是[261m/233g] ÷w×100%=261m/233w×100%。


科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O="O " dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A. (6a+5d-4c-12b)kJ·mol—1B(4c+12b-6a-5d)kJ·mol—1 B. (4c+12b-4a-5d)kJ·mol—1
C. (4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①菜籽油和氯化钠溶液 ②75%的医用酒精 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.过滤 萃取 分液
B.萃取 分液 蒸馏
C.分液 蒸馏 萃取
D.萃取 蒸馏 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的位置关系如图。下列说法一定不正确的是
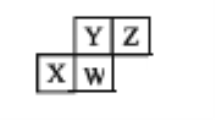
A. Z原子比X原子的最外层电子数多2个
B. 原子半径:W>X>Z>Y
C. 最高价氧化物对应的水化物的碱性:X>W
D. Y单质与氢气反应条件比Z单质更苛刻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法错误的是
A.PVC(聚氯乙烯)包装袋不能用于食品包装
B.能生成有机高分子化合物的反应只有加聚反应
C.糖尿病人应少吃含糖的食品,即使是未加糖的八宝粥也要慎重食用
D.塑料、合成橡胶和合成纤维称为三大合成材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年2月27日,昆明市一居民房因液化气泄漏引发火灾。已知液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是( )
A. 是直链烃,但分子中碳原子不在一条直线上
B. 在光照条件下能够与氯气发生取代反应
C. 丙烷比丁烷易汽化
D. 1 mol丙烷完全燃烧消耗5 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.从海水得到的粗食盐水中常含Ca2+、Mg2+、SO42-,需要分离提纯.现有含少量CaCl2、MgSO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂(1)盐酸、(2)Na2CO3、(3)NaOH、(4)BaCl2来除去食盐水中Ca2+、Mg2+、SO42-。提纯的操作步骤和加入试剂的情况如图1:

图中a、b、c、d分别表示上述4种试剂中的一种,试回答:
(1)生成沉淀A的化学方程式___________________________________;
(2)试剂d是________;判断试剂d已经足量的简单方法_______________________________;如果在加入d试剂前没有过滤,引起的后果是___________________________________。
(3)沉淀B、C、D的化学式分别为(不讲顺序)__________,_____________,____________;
(4)现有如图2仪器,过滤出沉淀A、B、C、D时必须用到______________(填序号)。

Ⅱ.海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的_______________________(填序号);实验时②中除加入适量海水外,还需加入_____,其作用是_________________________。
Ⅲ.海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述中的仪器,该仪器名称为____________。为了使该仪器中液体可以顺利流下,应进行的具体操作是__________。向该碘水中加入四氯化碳以提取碘单质的实验操作为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关卤族和碱金属元素性质的递变规律说法正确的是
A.卤族元素从F到I,对应氢化物的还原性逐渐增强
B.碱金属元素与O2反应均可得到多种氧化物
C.碱金属元素从Li到Cs,熔沸点逐渐升高
D.X2+2NaI=2NaX+I2(X为:F、Cl、Br)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com