
【题目】配制一定物质的量浓度的NaOH溶液时,可造成所配溶液浓度偏高的是( )
A. 所用NaOH已吸潮 B. 摇匀后液面低于刻度线,不再补加水
C. 有少量NaOH溶液残留在烧杯内 D. 向容量瓶加水至时刻度线时俯视液面
科目:高中化学 来源: 题型:
【题目】碘化钠是实验室中常用的分析试剂,也常用于医疗和照相业。工业上用铁屑还原法制备NaI,其主要流程如下图,请回答下列问题:

(1)试写出铁屑转化为Fe(OH)3的离子反应方程式:______________________________________。
(2)判断碘是否已完全反应的实验方法是______________________________________________。
(3)分离出NaI样品需在低温无氧环境中进行,其目的是__________________________________。
(4)测定产品中NaI含量的方法是:______________
a.称取3.000 g样品、溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用0.1000 mol/LAgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19.00 mL。
①上述测定过程所需仪器中,需要检查是否漏液的仪器有______________________________。
②上述样品中NaI的质量分数为__________________________。
(5)已知Ksp(AgI)=1.5×10-16,将AgNO3和NaI的溶液混合,假设混合液中AgNO3的浓度为0.01 mol/L,则开始生成AgI沉淀时,混合液中c( I- )=____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
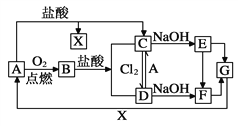
(1)写出A、C、F、G的化学式:A________,C_________,F_________,G_________。
(2)检验D中阳离子的方法_____________________________________________。
(3)保存C溶液时为什么要加固体A_____________________________________。
(4)写出下列转化的离子方程式C→D:____________________________________,由E转化为F的现象是 _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M2O7X-与S2- 在酸性溶液中发生如下反应:M2O7X-+3S2-+ZH+===YM3++3S↓+7H2O,则M2O7X-中M的化合价是( )
A. +4 B. +5 C. +6 D. +7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列诗句不涉及化学反应的是( )
A.爆竹声中一岁除,春风送暖入屠苏
B.飒飒西风满院栽,蕊寒香冷蝶难来
C.春蚕到死丝方尽,蜡炬成灰泪始干
D.开视化为血,衰今征敛无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为北京奥运会的奖牌﹣﹣“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )
A.Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO5MgO8SiO2H2O
B.从分类的角度看,Ca2Mg5Si8O22(OH)2为氧化物
C.玉石材料性质稳定,耐强酸和强碱的腐蚀
D.Ca2Mg5Si8O22(OH)2易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)CuS(s)+Mn2+(aq).一定温度下,下列有关该反应的推理正确的是( )
A.该反应达到平衡时c(Cu2+)=c(Mn2+)
B.平衡体系中加入少量CuS(s)后,c(Mn2+)变小
C.平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大
D.该反应的平衡常数K= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X是中学化学中的常见物质,存在如图所示转化关系(部分生成物和反应条件略去).

(1)若A为淡黄色粉末,则0.1molA与水反应时转移的电子数目为________.
(2)若A为常见的金属单质,焰色反应呈黄色;X是一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液的试剂为______________.
(3)若B具有漂白性,则A与H2O反应的离子方程式:________________.
(4)若A为红棕色气体,向E溶液中滴加足量氨水,生成的白色沉淀迅速变成绿色,最终变成红褐色.
①X的化学式为__________.
②A与H2O反应的化学方程式为____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应 A(g)+3B(g)2C(g)+2D(g),在不同情况下,测得有下列四个反应速率,其反应速率最快的是( )
A.v(A)=0.15molL﹣1s﹣1
B.v(B)=0.6molL﹣1s﹣1
C.v(C)=0.5molL﹣1s﹣1
D.v(D)=0.4molL﹣1s﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com