
【题目】下列实验基本操作(或实验注意事项)中,主要是从实验安全角度考虑的是
A. 实验剩余的药品一般不能放回原试剂瓶
B. 溶解时用玻璃棒搅拌
C. 可燃性气体点燃前必须验纯
D. 过滤时玻璃棒靠在三层滤纸处
科目:高中化学 来源: 题型:
【题目】在某未知溶液中加入硝酸银溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水中,石灰石变浑浊,由此判断该溶液中含有
A. Cl- SO42-B. Cl- NO3-C. Cl- CO32- D. Cl- OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存而且为无色透明的溶液是
A. NH4+,Al3+,SO42-,NO3-
B. K+,Na+,NO3-,CO32-,
C. K+,MnO4-,NH4+,NO3-
D. Na+,K+,HCO3-,NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.
则下列说法错误的是( )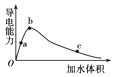
A.醋酸的电离程度:a<b<c
B.溶液的pH值:b<a<c
C.蘸取a点溶液滴在湿润的pH试纸上,测得pH值一定偏大
D.若分别取a、b、c三点的溶液各10 mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“塑料袋﹣﹣想说爱你不容易!”自1902年10月24 奥地利科学家马克斯舒施尼发明它以来,也只有短短的一百多年时间.这些花花绿绿、大大小小的塑料袋,不仅破坏城市景观,对环境的危害也是极惊人的.2008年6月1日起,根据国务院要求,所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用.下列说法正确的是( )
A.聚丙烯塑料的结构简式为 ![]()
B.聚氯乙烯塑料单体的电子式为 ![]()
C.塑料购物袋的生产原料需要消耗大量木材
D.聚乙烯中含碳质量分数与其单体的含碳质量分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种主族元素A、B、C、D、X、Y,其原子序数依次增大,均小于54;常温下A2B呈液态,是食物中主要营养物质之一;高纯C单质具有良好的半导体性能;D、X、Y原子核外最外层电子数均为7;过渡元素Z与B可形成多种化合物,其中红棕色粉末Z2B3常用作外墙涂料.请按要求回答下列问题:
(1)将D2水溶液滴入浅绿色的ZD2溶液中发生反应的离子方程式为 . ①学生甲认为X2和Y2都可能将Z2+氧化为Z3+ , 他推理的依据是 .
②而学生乙认为X2和Y2都不能将Z2+氧化为Z3+;学生丙认为X2能将Z2+氧化为Z3+而Y2不能.学生乙、丙推理的依据是 .
(2)A与B可形成既含极性键又含非极性键的化合物W.W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等.①W的电子式为 , W第一步电离方程式为 .
②如果配制W溶液的水中含有Z3+ , 会削弱W的消毒杀菌能力,甚至会完全失去杀菌作用.试用化学方程式分析其原因: .
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族,原子核外电子层数均小于7;常温下其单质,在空气中锡、锗不反应,而铅表面会生成一层氧化铅,锗与盐酸不反应,而锡与盐酸反应.由此可得出以下结论:①锗的原子序数为;
②它们+4价氢氧化物的碱性由强到弱顺序为(填化学式) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗甲流感药物达菲(Tamiflu)是以莽草酸(A)为原料,经过十步反应合成制得.莽草酸可以从常用的烹调香料“八角”中提取.达菲及A(莽草酸)、B的结构简式如图甲: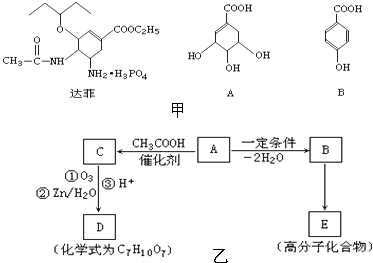
已知: ![]()
化合物A、B、C、D存在如图乙所示的转化关系:
回答下列问题:
(1)写出达菲中含氧官能团的名称:;
(2)写出A→C的反应类型:;
(3)写出B→E的化学方程式:;
(4)写出D的结构简式:;
(5)已知B有多种同分异构体,写出一种符合下列性质的B的同分异构体的结构简式①与FeCl3溶液作用显紫色;
②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种.
(6)设计A生成C的目的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是化合物,B是金属单质,它们之间相互反应以及生成物之间的转化关系如图所示: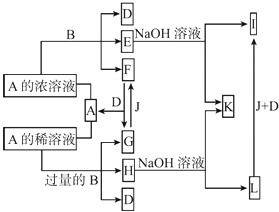
(1)金属B在元素周期表中的位置是 , B和A的浓溶液反应的条件是 . 写出少量B与A的稀溶液反应的离子方程式: .
(2)常温下0.1 mol/L E的水溶液中各离子浓度大小关系为 .
(3)L转化为I的现象是 . 写出有关的化学方程式: .
(4)如何检测H溶液中阳离子的存在,写出实验操作方法、现象、结论: .
(5)已知25℃时Fe(OH)3的Ksp=3.5×10﹣39 , 现将4.0×10﹣8 mol/L E溶液与2.0×10﹣8 mol/L NaOH溶液等体积混合(忽略溶液混合时体积的变化),通过列式计算说明是否有沉淀产生: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子最外层电子数与次外层电子数之比为3:4;N﹣、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体.据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式) .
(2)Z与M可形成常见固体化合物C,用电子式表示C的形成过程 .
(3)已知通常状况下1 g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热化学方程式 .
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式 .
(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1:1:1,A溶液中水的电离程度比在纯水中小.则化合物A中的化学键类型为;若B为常见家用消毒剂的主要成分,则B的化学式是 .
(6)均由X、Y、Z、M四种元素组成的两种盐发生反应的离子方程式是;其中一种是强酸所成的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com