
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( ) 
A.1:3
B.1:2
C.1:1
D.2:1
【答案】C
【解析】解:首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为10mL,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,生成Al(OH)3沉淀消耗的氢氧化钠溶液的体积=3×10mL=30mL,图象显示,生成沉淀总共消耗氢氧化钠溶液40mL,则生成氢氧化镁沉淀需要氢氧化钠的体积为10mL,
根据Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓知,镁离子和铝离子的物质的量之比为1:2,根据原子守恒知,Al2(SO4)3与MgSO4的物质的量浓度之比= ![]() =1:1,故选C.
=1:1,故选C.
首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为10mL,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的体积,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液40mL,计算沉淀Mg2+消耗的氢氧化钠溶液的体积,从而确定溶液中n(Mg2+):n(Al3+),再根据原子守恒确定其浓度之比.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】稀硝酸和铜反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,如果有3.2克铜和硝酸恰好完全反应,试计算:
(1)在标准状况下产生气体的体积是多少?
(2)将所得溶液加水配成200mL溶液,则溶液的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法利用了浓度对化学反应速率的影响的是
A. 将食物保存在电冰箱里B. 做粉尘爆炸实验时选用很细的面粉
C. 向过氧化氢溶液中加入MnO2D. 铁与稀盐酸反应太慢时加入较浓的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
(1)NO的物质的量为mol,NO2的物质的量为mol.
(2)待产生的气体全部释放后,向溶液中加入VmL、amolL﹣1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为molL﹣1 .
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要30%的双氧水g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素.它们在周期表的相对位置如下表:则下列说法正确的是( )
M | |||||||
X | Y | Z | |||||
W |
A.Y、M形成的气态化合物在标准状况下的密度为0.76 g.L﹣1
B.原子半径:W>Z>Y>X>M
C.由X元素形成的单质一定是原子晶体
D.XZ2、X2M2、W2Z2均为直线型的共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Mg、Al混合物投入200mL某浓度的盐酸中,金属完全溶解后,再逐滴加入2molL﹣1的 NaOH溶液至过量,所生成的沉淀与所加NaOH的关系如图所示: 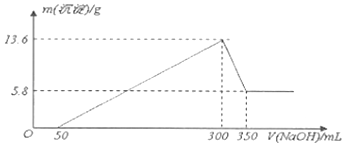
(1)0~50mL段内,发生反应的离子方程式为 .
(2)300~350mL段内,发生反应的离子方程式为 .
(3)试计算该盐酸的浓度.(写出必要的计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( ) 
A.实验中发生的反应都是化合反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体0.1 mol,完全燃烧得0.15 mol CO2和3.6 g H2O,下列关于该混合气体的说法正确的是
A. 一定有乙烯 B. 一定没有乙烯 C. 一定有甲烷 D. 一定有乙烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com