
�����������ѧ���õ��Լ�����ҵ�������̿��Ʊ���������������¡�
��1��д��ʵ��������KMnO4�ֽ���ȡO2�Ļ�ѧ����ʽ
��2��KMnO4ϡ��Һ��һ�ֳ��õ���������������ԭ��������������ͬ����
| A��84����Һ(NaClO��Һ) |
| B��˫��ˮ |
| C������ |
| D��75%�ƾ� |
��1��2KMnO4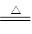 K2MnO4��MnO2��O2�� ��2�֣�
K2MnO4��MnO2��O2�� ��2�֣�
��2��AB ����1�֣���2�֣�ѡ�����÷֣�
��3����ʽ ��2�֣�
��4��3K2MnO4��2CO2 = 2KMnO4��2K2CO3��MnO2��2�֣�
��5�����ˣ�1�֣����ܽ�ȣ�1�֣���Ũ���ᾧ��1�֣�
��6��MnO2��1�֣���KOH��1�֣� 158��2�֣�
���������������1��ʵ��������KMnO4�ֽ���ȡO2�Ļ�ѧ����ʽ2KMnO4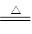 K2MnO4��MnO2��O2��
K2MnO4��MnO2��O2��
��2��KMnO4ϡ��Һ��һ�ֳ��õ���������������ԭ��������������ǿ�����ԡ�����������������ԭ����ͬ����A��84����Һ�������˴������ǿ�����ԣ���ȷ��B��˫��ˮ����ǿ�����ԣ���ȷ��C��������������������ʹϸ�������ʱ��ԣ�����D��75%�ƾ���������������ʹϸ�������ʱ��ԣ�����ѡAB��
��3����Ϊ������ؾ���ǿ�����ԣ���������ʽ�ζ�����ȡ��
��4�������������д����Ӧ�ٵĻ�ѧ����ʽ3K2MnO4��2CO2 = 2KMnO4��2K2CO3��MnO2
��5������Һ�������룬�ù��˵ķ��������Բ���1Ϊ���ˣ�KMnO4��K2CO3���������ܽ���ϲ������K2CO3���ܽ�ȸ������������ܽ�ȵIJ�ͬ������Ũ���ᾧ�����ȹ��˵õ�������ؽ��壻
��6��������ͼ�пɿ�����MnO2��KOH��ʼ���ģ��������ɣ����Կ�ѭ��ʹ�ã�����ѭ��ʹ�ã�����Ϊ��������ȫ��ת��Ϊ������أ���MnO2��KMnO4�����̿���MnO2��������87�֣����Կ�����KMnO4��������158�֡�
���㣺���鳣����������������ԭ��Ӧ����ѧ����Ͷ������Ʊ������⡢�����������Ի�ѧ����ʽ�ļ���


 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��) Mg(ClO3)2����������������ݼ��ȣ���ͼΪ�Ʊ�����Mg(ClO3)2��6H2O�ķ�����
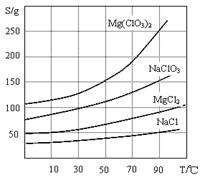
��֪��1��±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
2�����ֻ�������ܽ��(S)���¶�(T)�仯��������ͼ��
��1������BaCl2��Ŀ���dz�_________������жϸ������ѳ���_____________________��
��2������NaClO3������Һ�ᷢ����Ӧ��MgCl2��2NaClO3==Mg(ClO3)2��2NaCl���������ø÷�Ӧ������ܽ��ͼ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ��
��ȡ��������NaClO3������Һ��ַ�Ӧ��������Ũ������ ������ȴ�ᾧ��
�ݹ��ˡ�ϴ�ӣ����Mg(ClO3)2��6H2O���塣
��Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50g��Ʒ�ܽⶨ�ݳ�100mL��Һ��
����2��ȡ10mL��õ���Һ����ƿ�У�����10mLϡ�����20mL1.000mol/L��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100mol/L K2Cr2O7��Һ�ζ����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��
Cr2O72����6Fe2����14H��==2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7��Һ15.00mL��
��3��д������2����������Ӧ�����ӷ���ʽ ��
��4������3�����ζ�ǰ�ñ�Һ��ϴ�ζ��ܣ��ᵼ�����ս�� ���ƫ����ƫС�����䡱����
��5����Ʒ��Mg(ClO3) 2��6H2O����������Ϊ (������������λС��) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һƿ�������Һ�����п����� ��K����Na����Mg2����Ba2����Al3����Cl����I����
��K����Na����Mg2����Ba2����Al3����Cl����I���� ��
�� ��S2����
��S2���� ��
�� ��
�� ��ȡ����Һ��������ʵ�飺
��ȡ����Һ��������ʵ�飺
(1)ȡpH��ֽ���飬��Һ��ǿ���ԣ������ų� ���ӵĴ��ڣ�
(2)ȡ��������Һ����������CCl4������������ˮ������CCl4�����ɫ�������ų� ���ӵĴ��ڣ�
(3)��ȡ��������Һ��μ���NaOH��Һ��ʹ��Һ��������Ϊ���ԣ��ڵμӹ����к͵μ���Ϻ���Һ���������������ֿ����ų� ���ӵĴ��ڣ�
(4)ȡ����������������Һ�μ�Na2CO3��Һ���а�ɫ�������ɣ�֤�� ���Ӵ��ڣ��ֿ��ų� ���ӵĴ��ڣ�
(5)��(3)�õ��ļ�����Һ���ȣ�������ų�����������ʹʪ��ĺ�ɫʯ����ֽ��������������ʵ����ʵȷ��������Һ�п϶����ڵ������� ��������ȷ���Ƿ���ڵ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
V2O5�ǽӴ������������Ҫ��������ҵ������V2O5�Ĺ����������£���ش��������⣺
��1����������÷����ijɷ��� (д��ѧʽ)������NaOH��Һ��Ӧ�����ӷ�Ӧ����ʽΪ ��
��2������ڡ��۵ı仯���̿ɼ�Ϊ(��ʽR��ʾVO2+��HA��ʾ�л���ȡ��)��
R2(SO4)n(ˮ��)+2nHA(�л���) 2RAn(�л���)+nH2SO4(ˮ��)��
2RAn(�л���)+nH2SO4(ˮ��)��
��ʵ�����в���ڡ���ʹ�õ���Ҫ������ ��
������ȡʱ��������������ԭ���� ��
��3���������X�Լ�Ϊ ������ܵ�Ŀ���� ������ݵ����ӷ���ʽΪ ��
��4���ù��������У�����ѭ�����õ������� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ�ϳ�����ұ��п�����е�п������ZnO��FeO��Fe2O3��CuO��Al2O3�����ʣ�������������Zn(NO3)2��6H2O���壬�乤������Ϊ��
�й��������↑ʼ�����ͳ�����ȫ��pH���±���
| �������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| ��ʼ������pH | 3��3 | 1��5 | 6��5 | 4��2 | 5��4 |
| ������ȫ��pH | 5��2 | 3��7 | 9��7 | 6��7 | 8��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ�ϳ��ø�������Ч�ɷ�ΪFeO��Cr2O3����Ҫ����ΪSiO2��Al2O3��Ϊԭ�������ظ���أ�K2Cr2O7����ʵ����ģ�ҵ���ø��������ظ���ص���Ҫ������������ͼ���漰����Ҫ��Ӧ�ǣ�6FeO��Cr2O3��24NaOH��7KClO3=12Na2CrO4��3Fe2O3��7KCl��12H2O���Իش��������⣺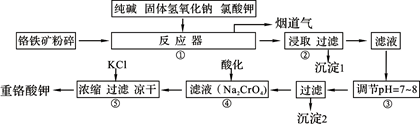
��1��������Һ���������ӵļ��鷽���� ��
��2������۱�����������Ϊ�������ӷ��ţ� ��
��3���ڷ�Ӧ�����У����������봿�Ӧ�Ļ�ѧ����ʽΪ�� ��
��4���̵����е�CO2����H2�ϳɼ״���CH3OH��H2��ȼ���ȷֱ�Ϊ����H=��725.5 kJ/mol����H=��285.8 kJ/mol��д����ҵ����CO2��H2�ϳ�CH3OH���Ȼ�ѧ����ʽ�� ��
��5��2011�����������ĸ���Ⱦ�¼���˵��������������ˮ���������ŷŶ��������滷���м����Σ������ⷨ�Ǵ�������Ⱦ��һ�ַ�������������������ʯī��������⺬Cr2O72-�����Է�ˮ��һ��ʱ������Fe(OH)3��Cr(OH)3������
��д����ⷨ������ˮ���ܷ�Ӧ�����ӷ���ʽ ��
����֪Cr(OH)3��Ksp=6.3��10�C31�����ر�ˮ�����������ֵ��0.1 mg/L��Ҫʹ��Һ��c(Cr3+)�������ϵر�ˮ��ֵ���������Һ��c(OH-)�� mol/L��ֻд�������ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1�������ӹ����θ�д����������ʽ��KAlSi3O8�� ��
��2����һ����ɫ��ĩ������K2SO4��NaHCO3��BaCl2��FeCl3��KCl���������е�ij������ɣ��ֽ�������ʵ�飺
�ٽ���ɫ��ĩ��ˮ�ܽ⣬����ɫ��Һ��
����������õ���ɫ��Һ�м���NaOH��Һ���۲쵽�а�ɫ����A���ɣ����˺�����Һ�еμ������ữ��AgNO3��Һ���ֵõ���ɫ����B��
�������������жϣ�
��A�Ļ�ѧʽ�� B�Ļ�ѧʽ�� ��
��ԭ��ɫ��ĩ��һ������ �����ܺ��� ��
�Կ��ܺ��е����ʣ���ͨ�� ����ʵ�����ƣ���һ�����顣������������У���պȡ����Һ�������ھƾ��ƻ��������գ�������ɫ�ܲ����۲죻����ϡ����ϴ����˿��������ȷ�IJ���˳��Ϊ ��
A���٢ڢۢ� B���ܢ٢ڢ� C���ܢڢ٢ڢۢ� D���٢ۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������̿������ɵ��ȥ�������ϳɹ�ҵ�Ĵ�������������������ҵ���´ɹ�ҵ����ɫ������ɫ�����������ȡ�
��1���������������Խ�������һ��ǿ�����������û�ѧ����ʽ֤����______________________��
��2��п���̼��Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�á���ص��ܷ�ӦʽΪZn��s����2MnO2��s����H2O��l��=Zn��OH��2��s����Mn2O3��s����
�ٵ�ع���ʱ��MnO2����________��Ӧ��
�ڵ�ص�������ӦʽΪ________��
��3����ҵ�������̿�Ϊԭ�ϣ��������������Ʊ��ߴ��������̵��������£�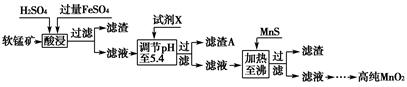
��֪�����̿����Ҫ�ɷ�ΪMnO2������Si��16.27%����Fe��5.86%����Al��3.42%����Zn��2.68%����Cu��0.86%����Ԫ�صĻ��������������������������������ʽ��ȫ����ʱ��Һ��pH���±���
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Mn��OH��2 | Cu��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 |
| ������ | Zn��OH��2 | CuS | ZnS | MnS | FeS |
| pH | 8.0 | ��0.42 | 2.5 | 7 | 7 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com