
T Kʱ����2.0 L�����ܱ������г���1.0 mol COCl2����ӦCOCl2(g) Cl2(g)��CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
Cl2(g)��CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
| t / s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2) / mol | 0 | 0.16 | 0.19 | 0. 20 | 0.20 |
CD
�������������A�����и��������������ʵ�������Ӧ���������ʵ���Ũ�ȼ��㣬v(CO)= 0.040mol��L��1��s��1������B��ƽ��ʱc(Cl2)=" 0.10" mol��L��1�������¶�Ũ�ȱ��Ӧ������У��ʦ�H>0������
C�� COCl2(g) Cl2(g)��CO(g)
Cl2(g)��CO(g)
��ʼŨ�� 0.5 0 0
ת��Ũ�� 0.1 0.1 0.1
ƽ��Ũ�� 0.4 0.1 0.1
k="0.1��0.1��0.4=0.025"
Q=0.05��0.05��0.45��0.006
K��Q���ʷ�Ӧ������У�v��>v������ȷ��
D��T Kʱ��ʼ�������г���1.0 mol Cl2��1.0 mol CO�������1.0 mol COCl2�ǵ�Чƽ�⣬�ﵽƽ��ʱŨ����ͬ����CO���٣�ƽ��������У�Cl2ת���ʽ��ͣ���ȷ��
���㣺���黯ѧƽ����ƶ����йؼ�������ݡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ϳɰ��������������ú��ˮ��ԭ�Ͼ��ಽ��Ӧ�Ƶã����е�һ����ӦΪ��
CO(g)��H2O(g)  CO2(g)��H2(g) ��H<0
CO2(g)��H2(g) ��H<0
��Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ����д�ʩ����ȷ����( )
| A������ѹǿ | B�������¶� | C������CO��Ũ�� | D���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������н��з�Ӧ��2A��g��+B��g�� 3C��g����Q(Q��0)�����и�ͼ��ʾ��������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
3C��g����Q(Q��0)�����и�ͼ��ʾ��������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����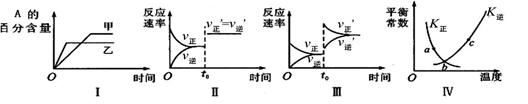
| A��ͼI��ʾ�¶ȶԻ�ѧƽ���Ӱ�죬�Ҽ��¶Ƚϸ� |
| B��ͼ���ʾt0ʱ����С��������Է�Ӧ���ʵ�Ӱ�� |
| C��ͼ���ʾt0ʱ������BŨ�ȶԷ�Ӧ���ʵ�Ӱ�� |
| D��ͼ����a��b��c������ֻ��b���Ѿ��ﵽ��ѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�й�����ͼ���˵����ȷ����
| A������ͼ�ٿ��Ա�ʾ��ij��ѧƽ����ϵ�ı��¶Ⱥ�Ӧ������ʱ��ı仯 |
| B������ͼ���жϣ�����A��Ӧ��������C�ġ�H>0 |
| C������ͼ�ۿɱ�ʾ��һ������������Һ�еμ�һ��Ũ������������Һʱ��pH�仯 |
| D������K����A��B�����ɼ������ĸ�ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��CoCl2�ܽ���Ũ�����У���Һ�д�������ƽ�⣺
Co2+ + 4Cl�� CoCl4�� ��H��0
CoCl4�� ��H��0
�ۺ�ɫ ��ɫ
�й��������淴Ӧ������˵������ȷ���� �� ��
| A������Һ������ϵ���ȣ���Һ��ɫ���� |
| B������Һ������ϵ�ñ�ˮ���£�������Ӧ��ƽ�ⳣ����С |
| C�������£���ˮϡ�ͣ�������Ӧ��ƽ�ⳣ����С |
| D�������£���ˮϡ����һ����Χ����ҺΪ�ۺ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
Ϊ��СCO2�Ի�����Ӱ�죬�ڳ�������̼����ͬʱ�������ǿ��CO2�������õ��о���T10C ʱ����9molCO2��12molH2����3L�ܱ������У�������ӦCO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H<0��������CH3OH�����ʵ�����ʱ��仯������I��ʾ��ƽ��ʱ������ѹǿΪP���ı�ijһ�������½���������Ӧ,CH3OH�����ʵ�����ʱ��仯������II��ʾ������˵���������
CH3OH(g)+H2O(g) ��H<0��������CH3OH�����ʵ�����ʱ��仯������I��ʾ��ƽ��ʱ������ѹǿΪP���ı�ijһ�������½���������Ӧ,CH3OH�����ʵ�����ʱ��仯������II��ʾ������˵���������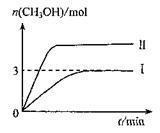
| A������II��Ӧ�������ı�������ѹǿ |
| B��T2��Cʱ��������Ӧƽ�ⳣ��Ϊ0.42����T2> T1 |
| C����T10C������ʼʱ�������г���5 mol CO2��5 mol H2��5 mol CH3OH(g)��5 mol H2O(g)�����ƽ��ǰv(��)>v(�棩 |
D����T10C������ʼʱ��������ͨ��4,5 molCO2��6mol H2 ,ƽ��ʱ������ѹǿ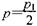 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��xA(g)+B(g) 2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ �� ��
| ���� | �� | �� | �� |
| �ݻ� | 0.5L | 0.5L | 1. 0L |
| �¶ȣ� | T1 | T2 | T3 |
| ��Ӧ�� ��ʼ�� | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
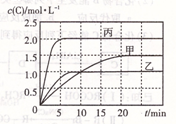
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ݻ�Ϊ2L���ܱ������н��з�Ӧ��CO(g)+2H2(g) CH3OH(g)�������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ������˵����ȷ����
CH3OH(g)�������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ������˵����ȷ����
| A���÷�Ӧ�ġ�H<0 |
| B�������������䣬�����¶ȷ�Ӧ��ƽ�ⳣ������ |
C��300��ʱ��0�Ct1 min��CH3OH��ƽ����������Ϊ mol?L��1 min��1 mol?L��1 min��1 |
D��A��ķ�Ӧ��ϵ��300�����ߵ�500�棬�ﵽƽ��ʱ ��С ��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���д�ʩ�У��ܼ�����ѧ��Ӧ���ʵ���
| A��ʳ�ﴢ���ڱ����� |
| B������״����ҩƷ��ϸ���ٷ�Ӧ |
| C����MnO2��H2O2�ֽⷴӦ�Ĵ��� |
| D����30%H2SO4��Һ����5%H2SO4��Һ��п����Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com