
天然碱的组成可以用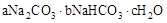 (a、b、c为整数)表示。现有A、B两种不同的天然碱样品,分别进行如下实验以确定其化学式。
(a、b、c为整数)表示。现有A、B两种不同的天然碱样品,分别进行如下实验以确定其化学式。
将质量为31.0 g的天然碱A于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2 2.24 L(标准状况)和水5.4 g。
(1)天然碱A的化学式中: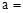
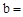

已知:Na2CO3与稀盐酸的反应分下列两步进行:
Na2CO3+HCl NaCl+NaHCO3 NaHCO3+HCl
NaCl+NaHCO3 NaHCO3+HCl NaCl+CO2↑+H2O
NaCl+CO2↑+H2O
将质量为12.45 g的天然碱B溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐
酸的体积(标准状况)的关系如下表所示:
| 盐酸体积(mL) | 20 | 40 | 60 | 80 |
| 产生气体体积(mL) | 0 | 560 | 1680 | 2520 |
(1)a=1,b=2,c="2" (各1分,共3分)
(2)1120mL(2分) ; 2.5mol/L (2分) ;2Na2CO3·NaHCO3 ·2H2O (3分)
(3)0g<W≤4.98g V="67200W/332" mL(或V=202.41WmL)
4.78g<W<12.45g V=1680﹣44800W/332 mL (或V=1680﹣134.94W mL)
W≥12.45g V=0mL
解析试题分析:(1)利用2NaHCO3 Na2CO3+CO2↑+H2O 这个原理。由题意可知n(CO2)=0.1 mol。
Na2CO3+CO2↑+H2O 这个原理。由题意可知n(CO2)=0.1 mol。
2NaHCO3 Na2CO3+ CO2↑+ H2O
Na2CO3+ CO2↑+ H2O
2 1 1 1
0.2 mol 0.1 mol 0.1 mol 0.1 mol
m(NaHCO3)="0.2" mol×84 g·mol-1="16.8" g,所以晶体中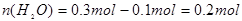 ,m(H2O)="0.2" mol×18 g·mol-1="3.6" g,m(Na2CO3)=31 g-16.8 g-3.6 g=10.6 g,
,m(H2O)="0.2" mol×18 g·mol-1="3.6" g,m(Na2CO3)=31 g-16.8 g-3.6 g=10.6 g,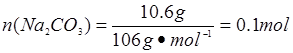 。由此可知晶体中n(Na2CO3)∶n(NaHCO3)∶n(H2O)=0.1 mol∶0.2 mol∶0.2 mol=1∶2∶2。所以晶体化学式为Na2CO3·2NaHCO3·2H2O。
。由此可知晶体中n(Na2CO3)∶n(NaHCO3)∶n(H2O)=0.1 mol∶0.2 mol∶0.2 mol=1∶2∶2。所以晶体化学式为Na2CO3·2NaHCO3·2H2O。
(2)①Na2CO3与盐酸反应分步进行。首先发生:Na2CO3+HCl="NaCl+" NaHCO3.当Na2CO3完全转化为NaHCO3后,发生NaHCO3+HCl=NaCl+H2O+CO2↑。若固体只含有Na2CO3,则前后两步消耗的盐酸物质的量相等。由56题由40到60ml当盐酸体积增大了20ml时气体体积增加了1120ml,故加入50mL盐酸时,盐酸体积增加了10ml时,产生气体的体积就增加了560ml,即为1120ml。由表中数据当盐酸体积由60到80ml增加20ml时,气体的体积只增加了840ml,说明此时盐酸过量,12.45克B完全反应完。可以求出n(CO2)=2520/22.4=0.1125mol,再由20ml盐酸产生气体1120ml,即为0.5mol,此时发生的反应为NaHCO3+HCl=NaCl+H2O+CO2↑,可知盐酸的物质的量为0.5mol,则浓度为0.5/0.02= 2.5mol/L。由数据盐酸体积40ml对应气体体积560ml,进行分析,盐酸不中,固体剩余。n(HCl)=0.1 mol,B中碳酸钠物质的量为x,则碳酸氢钠为0.1125-x,和碳酸钠反应掉的盐酸为xmol,和碳酸氢钠反应的盐酸为0.1-x,则有0.1-x="0.025" x=0.075mol,即碳酸钠质量为0.075*106=7.95g,碳酸氢钠为0.1125-x=0.1125-0.075=0.0375mol,质量为3.15g,水的质量为1.35g,物质的量为0.075mol。n(Na2CO3)∶n(NaHCO3)∶n(H2O)=0.075mol∶0.0375 mol∶0.075mol=2∶1∶2。
(3)当盐酸与天然碱恰好完全反应生成CO2时,天然碱2Na2CO3?NaHCO3?2H2O的摩尔质量为332g?mol-1,每摩尔天然碱消耗盐酸5mol,则样品质量为:(0.03×2.5×332)/5g=4.98g;当样品过量,Na2CO3恰好转化为NaHCO3而没有生成CO2时,样品质量为:(0.03×2.5×332)/2g=12.45g。然后在0<m≤4.98、4.98<m≤12.45、1245≤m三个区间讨论计算即可。
考点:考查质量守恒定律、氧化还原反应方程式的书写、碳酸钠与盐酸的分步反应等知识。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:填空题
标准状况下336 L的NH3溶于1 L水中,所得溶液的质量分数为________,若该溶液的密度为a g/cm3,则物质的量浓度为________。将上述氨水全部转化为NH4Cl,所需4 mol·L-1的盐酸的体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
闪锌矿(主要成份为ZnS)是含锌主要矿物之一,空气中高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。回答下列问题(以下计算保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留
固体的质量为1.32 g,样品中含硫化锌的质量分数是_________。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液中和余酸,耗用NaOH溶液的体积为21.70 mL。
①反应后溶液中多余的硫酸是____________ mol。
②通过计算确定浓硫酸被还原的产物是________________________。
(3)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
向10mLNa2CO3和Na2SO4的混合溶液中加入足量的氯化钡溶液,生成沉淀的质量为6.27g,向所得沉淀中加入足量稀盐酸,沉淀质量减少到2.33g,并放出气体,试计算:
(1)原混合物中Na2SO4的物质的量浓度为 mol?L-1;
(2)在标准状况下产生气体的体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室配制500 mL 0.2 mol·L-1的Na2SO4溶液,实验操作步骤有:
A.在天平上称出14.2 g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却 至室温。
B.把制得的溶液小心地转移到容量瓶中。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶瓶塞塞紧,充分摇匀后装瓶。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)____ _。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是________、________。
(3)下列情况会使所配溶液浓度偏高的是(填序号)______ __。
A.容量瓶使用前内壁沾有水珠 B.没进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线 D.砝码上沾有杂质
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室配制480 mL 0.1mol·L-1 NaOH溶液,回答下列问题
(1)应用托盘天平称取氢氧化钠固体 g。
(2)配制NaOH溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒 、 。
使用容量瓶前必须进行的操作是 。
(3)配制时,该实验两次用到玻璃棒,其作用分别是 、 。
(4)定容时若加水超过刻度线,应如何处理? 。
(5)试分析下列操作对所配溶液的浓度有何影响。
A. 偏高 B. 偏低 C.不变(用符号回答)
① 定容时俯视刻度线 ;
② 放在滤纸上称量NaOH固体 。
③容量瓶没有干燥,有少量蒸馏水: 。
④定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度: 。
(6)请你帮助把试剂瓶(盛放上述配制好的溶液)上标签的内容填上去 (标签如图)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)0.5molCH4的质量是 g,在标准状况下的体积为 L;含 有约 个氢原子。
将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为 ;配制300 mL 0.5 mol·L-1氯化钠溶液,需要1.5 mol·L-1的氯化钠溶液的体积是 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)3.01×1022个OH- 的物质的量为________,质量为________,含有质子的物质的量为________,含有电子的物质的量为________。
(2)相同状况下,10mL X2气体与30mL Y2气体化合生成20mL C气体,则C的化学式为_________。
(3)某地酸雨经检验,除含氢离子外,还有如下离子:c(Na+)=1.4×10-3 mol·L-1 ,
c(Cl- ) =3.5×10-3 mol·L-1,c(NH4+) =2.3×10-3 mol·L-1, c(SO42-) =1.5×10-3
mol·L-1。则该溶液中氢离子的浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)按要求填空:
(1)以下物质:①NH3 ②CaCO3 ③酒精 ④饱和食盐水 ⑤Cu ⑥KOH ⑦HCl属于电解质的有 (填编号);
(2)14.7gH2SO4分子所含氢原子数与 L (标准状况下)NH3所含氢原子数相等;
(3)固体NaCl(I2)(括号内的物质为杂质),除去杂质的方法为 。
(4)要除去某食盐晶体中的CaCl2、MgCl2、Na2SO4等杂质,有以下操作:
| A.蒸发结晶 | B.过滤 | C.加入过量的Na2CO3溶液 | D.加水溶解 E、加入过量的烧碱溶液 F、加入过量稀盐酸 G、加入过量的Ba(NO3)2溶液 H、加入过量的稀硝酸 I、加入过量的BaCl2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com