
【题目】对于反应2A(g)+B(g)![]() 2C (g)ΔH<0,下列图象正确的是( )
2C (g)ΔH<0,下列图象正确的是( )
A.  B.
B. 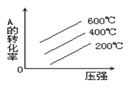
C.  D.
D. 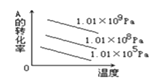
【答案】D
【解析】
反应2A(g)+B(g)2C(g)为气体体积缩小的反应、△H<0说明反应为放热反应,则升高温度,平衡逆向移动,增大压强,平衡正向移动,结合图像分析解答。
A.温度越高,反应速率越快,建立平衡需要的时间越少,与图像一致;但升高温度,平衡逆向移动,B的物质的量分数增大,与图像不符,故A错误;
B.增大压强,平衡正向移动,A的转化率增大与图像一致;但升高温度,平衡逆向移动,A的转化率减小与图像不符,故B错误;
C.增大压强,平衡正向移动,C的物质的量分数增大与图像一致;但升高温度,平衡逆向移动,C的物质的量分数应减少与图像不符,故C错误;
D.增大压强,平衡正向移动,A的转化率增大与图像一致;升高温度,平衡逆向移动,A的转化率减小与图像一致,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用氯气.
I.工业上通常采用电解法制氯气:观察下图,回答:
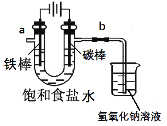
(1)电解反应的化学方程式为____________________。
(2)饱和食盐水通电后,b端产生的气体检验方法是____________。
II. 实验室用NaOH固体配制100 mL 1.0 mol·L-1的NaOH溶液,试回答下列各题:
(3)需要用托盘天平称量_______g NaOH固体;
(4)实验室有下列仪器:①漏斗 ②200mL容量瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥托盘天平 ⑦冷凝。若要实施溶液配制,尚缺的玻璃仪器是___________、________;
(5)容量瓶在使用前必须先____________;
(6)配制过程有以下操作: ①称量 ②移液 ③冷却 ④洗涤 ⑤定容 ⑥溶解 ⑦摇匀 其正确的操作顺序应是:① →_________→________ →________ →________→________→ ⑦
(7)下列五项操作中会导致所得溶液浓度偏低的有____________(填序号);
①没有洗涤烧杯内壁和玻璃棒
②未冷却到室温就将溶液转移到容量瓶并定容
③在转移过程中有溶液撒在外面
④定容时观察液面时俯视
⑤定容后,把容量瓶反复摇匀后发现液面低于刻度线,便滴加几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中:①SO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水。能导电的是__________(填序号,下同)。属于电解质的是__________。属于非电解质的是__________。
(2)1.204×1024个H2SO4分子的物质的量为__________mol,共含__________个氢原子。将上述H2SO4溶于水配成600 mL溶液,再加水稀释到1000 mL,稀释后溶液的物质的量浓度为__________mol/L。
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为__________mol/L。
(4)有以下四种物质:① 标准状况下11.2 L CO2 ② 5 g H2 ③ 1.204×1024个N2分子 ④ 18 g H2O,其中质量最大的是____(填序号),在常温常压下体积最大的是___(填序号)。
(5)标准状况下11.2 L由CH4、N2组成的混和气体的质量为10 g,该混合气体中CH4与N2的分子数之比为_________。
(6)将标准状况下336 L HCl气体完全溶于1 L水中,所得溶液的密度为 ρ g/cm3,则该溶液的物质的量浓度为_____ mol/L(计算结果中的数字保留整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的有效利用可以缓解温室效应和能源短缺问题。
(1)CO2的分子结构决定了其性质和用途。
①CO2的电子式是_____________。
②在温度高于31.26 ℃、压强高于7.29×106Pa时,CO2处于超临界状态,称为超临界CO2流体,它可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,用超临界CO2萃取的优点有:___________(答出一点即可)。
(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。

上图中CO2转化为CO的反应为:CO2(g)+H2(g) = CO(g)+H2O(g) △H= +41kJ/mol
已知:2CO2(g)+6H2(g) = C2H4(g)+4H2O(g) △H= -128kJ/mol
①则图中CO转化为C2H4的热化学方程式是____________________。
②关于X与Y的说法正确的是________(填序号〕。
a.实验式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.互为同系物
③催化剂中Fe3O4的制备方法如下:将一定比例的FeCl2和FeCl3溶于盐酸,然后在 60 ℃下逐滴加入NaOH溶液至pH≈10,继续搅拌,得Fe3O4。该反应的离子方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种自热食品的自热包上标注的成分是铝粉、生石灰、小苏打,自热包打开后加水即可大量放热。加水过程中发生的主要反应不可能是
A. 2Al+Ca(OH)2+2H2O=Ca(AlO2)2+3H2↑
B. Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O
C. 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
D. CaO+H2O=Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(MnS)=2.5×10-13,常温下三种物质在水中的沉淀溶解平衡线如图所示(X表示Fe、Cu、Mn)。下列说法正确的是

A. 曲线Ⅰ表示CuS的溶解平衡曲线
B. MnS在a点溶液中的溶度积等于在b点溶液中的溶度积
C. c点与d点溶液中S2-的物质的量浓度相等
D. 向含有XS固体的d点溶液中滴加稀硫酸至过量可使固体逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯(结构如图1所示)是食品行业中常用的一种香精,柠檬烯熔点为-74.3℃,沸点为177℃,难溶于水,在接近100℃时有一定的挥发性。柠檬、橙子和柚子等水果果皮中存在较多的柠檬烯,实验室通常用水蒸气蒸馏(装置如图2所示)的方法将柠檬烯从果皮中提取出来并进行后续的分离提纯。
水蒸气蒸馏:将60g橙子皮剪成碎片投入仪器B中,加入30mL蒸馏水,打开T形管活塞,点燃酒精灯加热水蒸气发生装置,待T形管支管口有大量水蒸气冒出时关闭活塞并开始通入冷凝水,当D中收集到约60~70mL馏出液时停止蒸馏。
分离提纯:将馏出液倒入分液漏斗,每次用10mL二氯甲烷(沸点39.95℃)萃取三次,萃取液合并后置于锥形瓶中,加入适量无水硫酸镁,半小时后过滤,将滤液进行蒸馏除去二氯甲烷,蒸馏烧瓶中得到主要成分是柠檬烯的橙油。
请回答相关问题。

(1)仪器A的名称是____。安全管下端不能抵住仪器A的底部,原因是__。仪器B中水蒸气导入管管口接近瓶底,目的是___。
(2)直形冷凝管填能否更换为球形冷凝管___(“能”或“否”),原因是___。
(3)分离提纯过程中加入无水硫酸镁的作用是____。对滤液进行蒸馏时合适的加热方法是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100 mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成2.4 g硫单质、0.425 mol FeCl2和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是 ( )
A. 100 mL的盐酸中HCl的物质的量浓度为7.5 mol·L-1
B. 生成的H2S气体在标准状况下的体积为2.24 L
C. 该磁黄铁矿FexS中,x=0.85
D. 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com